
实验室常利用此反应制取少量氮气:NaNO2+NH4Cl=NaCl+N2↑+2H2O制备N2,下列说法正确的是
A.NaNO2氧化剂
B.每生成1mol N2转移电子的物质的量为6mol
C.NH4Cl中的氮元素被还原
D.N2既是氧化剂,又是还原剂
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知YW的原子充数之和是Z的3倍,下列说法正确的是
Y | Z | ||
X | W |
A.原子半径:X<Y<Z
B.气态氢化物的稳定性:X>Z
C.Z、W均可与Mg形成离子化合物
D.最高价氧化物对应水化物的酸性:Y>W
查看答案和解析>>
科目:高中化学 来源:2016届安徽省皖南八校高三上学期第一次联考化学试卷(解析版) 题型:推断题
a、b、c、d代表四种短周期主族元素。已知:a、b、c同周期,且原子序数之和为22;元素b的最简单氢化物与元素a的氢化物可化合生成离子化合物M;d是短周期中金属性最强的元素.b的最高和最低化合价的代数和为2。
请回答下列问题:
(1)a、b、c的元素符号依次为_______、_______、_______。d在氧气中燃烧产物的电子式为 。
(2) 三种常见离子,在化合物M的水溶液中不能大量存在的是 (填离子符号)。
三种常见离子,在化合物M的水溶液中不能大量存在的是 (填离子符号)。
(3)元素e为a的同主族短周期元素,e的单质可与水反应,写出反应的离子方程式:______________
(4)c的一种氢化物的相对分子质量为78,是英国科学家法拉第在1825年首先发现的,分子中两种元素的原子个数比为1:1,该氢化物的分子中有 个原子共平面,写出该氢化物与e的单质在氯化铁催化作用下发生取代反应的化学方程式:____ 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上期中测试化学试卷(解析版) 题型:选择题
用NA表示阿伏伽德罗常数的值。下列判断正确的是
A.28g N2含有的氮原子数目为NA
B.常温常压下,22.4L Cl2含有的分子数目为NA
C.1molNa变为Na+时失去的电子数目为NA
D.1L 1mol·L—1K2CO3溶液中含有的钾离子数目为NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第一次月考化学试卷(解析版) 题型:选择题
将4molA和2molB在2L密闭容器中混合发生反应,2A(g)+B(g) 2C(g);ΔH<0,4秒后反应达到平衡状态,此时得C的浓度为0.6mol/L,下列说法正确的是
2C(g);ΔH<0,4秒后反应达到平衡状态,此时得C的浓度为0.6mol/L,下列说法正确的是
A.当A、B、C物质的量浓度化为2︰1︰2时,反应即达到平衡状态
B.4S内用物质B表示的反应速率为0.075mol/(L·S)
C.达平衡后通入一定量的氦气,A的转化率降低
D.达平衡后升高温度,C的浓度将增大
查看答案和解析>>
科目:高中化学 来源:2016届福建省大田市高三上学期第一次月考化学试卷(解析版) 题型:填空题
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
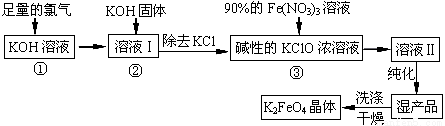
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH 与Cl2 反应生成的是KClO3。写出在温度较高时KOH 与Cl2反应的化学方程式 ,当反应中转移5 mol电子时,消耗的氯气是 mol。
(2)在反应液I中加入KOH固体的目的是 (填编号)。
A.与反应液I中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3 、KCl,则反应③中发生的离子反应方程式为 。
(4)如何判断K2FeO4晶体已经洗涤干净 。
(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,其离子反应是: FeO42? + H2O = Fe(OH)3(胶体) + O2↑ + ,完成并配平上述反应的离子方程式。
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第一次月考化学试卷(解析版) 题型:填空题
(每空1分,共11分)从下列各组反应对比,判断那种微粒的氧化性最强。
(1)铁钉浸入硫酸铜溶液中后,表面会附有红色物质,铜丝浸入硝酸银溶液后,表面会附有银白色物质。则铜、铁、银中,_____ ___原子的还原性最强;Cu2+、Ag+、Fe2+中, 离子的氧化性最强。
(2)在氯气中Fe锈蚀成棕褐色物质FeCl3,而在盐酸中生成淡绿色溶液FeCl2。则氯气分子、氢离子、氯离子中, 具有氧化性, 氧化性最强。请书写出以上各反应的化学方程式________ 、 。
(3)已知在ⅣA族元素中,Pb2+和Sn4+的化合物较为稳定。
①据此可判断PbO2具有较强的________性,SnCl2具有较强的 性;写出PbO2溶于盐酸的离子方程式__________;写出SnCl2和FeCl3溶液混合的离子方程式__________ ;
②PbO2、Fe3+、Cl2、Sn4+氧化性由强到弱的顺序是__________ 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期第一次月考化学试卷(解析版) 题型:选择题
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积, ③溶液的温度,④氯离子的浓度,影响反应速率的因素是

A.①④ B.③④ C.②③ D.①②③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上学期期中测试化学试卷(解析版) 题型:计算题
实验室常用加热高锰酸钾的方法制取少量氧气。
(1)请写出反应的化学方程式
(2)现欲制取2.24L(标准状况)的氧气,需要消耗高锰酸钾多少克?
(3)生成的二氧化锰的物质的量是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com