
分析 同一容器在同一条件下盛放不同的气体时,所含分子数必然相等,NO和H2按相同物质的量混合时,气体的平均相对分子质量为$\frac{30+2}{2}$=16,而SO2的相对分子质量为64,则相同体积SO2的与NO和H2的混合气体的质量为4:1,据此解答.
解答 解:同一容器在同一条件下盛放不同的气体时,所含分子数必然相等,NO和H2按相同物质的量混合时,气体的平均相对分子质量为$\frac{30+2}{2}$=16,而SO2的相对分子质量为64,称量物品质量时,砝码应放在天平的右盘,设密闭容器内气体的物质的量为n,则盛满以相同物质的量混合的NO和H2的混合气体后,气体的质量为16n=Q,n=$\frac{Q}{16}$,当充满SO2气体时,气体的质量为:m=64n=64×$\frac{Q}{16}$=4Q,容器的总质量为M+4Q,
故答案为:右;M+4Q.
点评 本题考查阿伏伽德罗定律及其推论,根据PV=nRT理解阿伏伽德罗定律及其推论进行计算即可解答,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 戊二醛分子式为C5H10O2,符合此分子式的二元醛有4种 | |
| B. | 戊二醛不能在加热条件下和新制备的氢氧化铜反应 | |
| C. | 戊二醛不能使酸性KMnO4溶液褪色 | |
| D. | 2%的GA溶液能破坏菌体蛋白质,杀死微生物,具有消毒杀菌作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在此过程中,NO2是氧化剂 | |
| B. | 在此过程中,NO是反应的中间产物 | |
| C. | 该过程总反应的化学方程式为2O3═3O2 | |
| D. | 光化学烟雾能引起人严重的呼吸功能障碍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第14列元素的最高价氧化物的化学式为RO2 | |
| B. | 第2列元素中一定没有非金属元素 | |
| C. | 在18列元素中,第3列元素种类最多 | |
| D. | 第15列元素的最高价氧化物对应水化物的化学式均为H3RO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
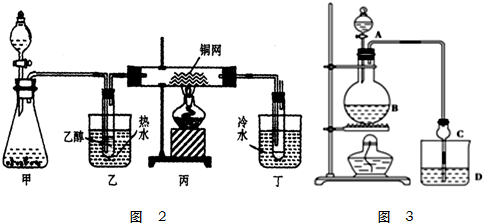
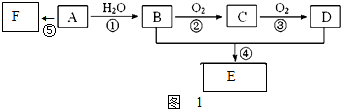 已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②经查阅资料得知:2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH.
已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②经查阅资料得知:2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH.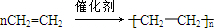
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V1>V2 | B. | V1<V2 | C. | V1=V2 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
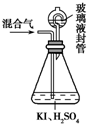 用如图装置可以测定混合气中ClO2的含量:
用如图装置可以测定混合气中ClO2的含量:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com