
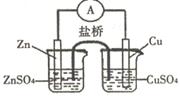
| A.电子从锌电极通过电流表流向铜电极 |
| B.盐桥中的阴离子向硫酸铜溶液中迁移 |
| C.取出盐桥后,电流计的指针仍发生偏转 |
| D.铜电极上发生的电极反应是2H+ + 2e- = H2↑ |


科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
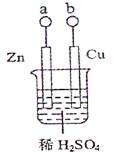
| A.a、b不连接时,只有锌片上有气泡逸出 |
| B.a和b用导线连接时,铜片上发生的反应为:2H+ + 2e-=H2 ↑ |
| C.a和b是否用导线连接,装置中所涉及的化学反应都相同 |
| D.a和b用导线连接或接直流电源,锌片都能溶解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
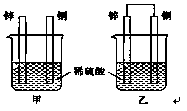
| A.装置甲、乙中铜片表面均无气泡产生 |
| B.装置甲、乙中稀硫酸的浓度均减小 |
| C.装置乙中锌片是正极,铜片是负极 |
| D.装置乙中产生气泡的速率比装置甲快 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
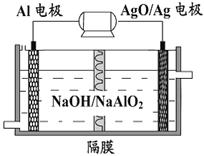
| A.有Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3 e-=Al3+ |
| B.Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3 e-=Al3+ |
| C.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Fe-2e-═Fe2+, |
| D.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.锌锰干电池是一种常用的二次电池 |
| B.氢氧燃料电池比火力发电的能量转变率要高 |
| C.锌锰干电池工作一段时间后锌外壳逐渐变薄 |
| D.碱性燃料电池正极反应是O2 + 2H2O + 4e- =4OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
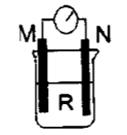
| | M | N | R |
| A | 锌 | 铜 | 稀硫酸 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 银 | 锌 | 硝酸银 |
| D | 锌 | 铜 | 硫酸铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温条件下,在空气中铝不容易被腐蚀 |
| B.镀锌铁片比镀锡铁片更耐腐蚀 |
| C.用锌与硫酸制氢气时,往硫酸中滴少量硫酸铜 |
| D.远洋海轮的尾部装上一定数量的锌板 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com