
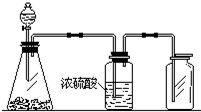
 如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是( )
如图是一套实验制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是( )| A. | 制取NO气体 | B. | 制取二氧化碳气体 | ||
| C. | 制取氯气 | D. | 制取氨气 |
分析 由装置图可知,反应为液体和固体的反应,且不需要加热,生成的气体可用浓硫酸干燥,且能用向上排空法收集,说明气体的密度比空气大,不与空气中氧气发生反应,以此解答该题.
解答 解:A.铜和稀硝酸反应生成的NO密度和空气非常接近,难溶于水,与空气中的氧气反应,所以只能用排水法收集,故A错误;
B.大理石和稀盐酸反应生成二氧化碳,二氧化碳密度比空气大,可用向上排空法收集,故B正确;
C.高锰酸钾和浓盐酸应在不加热的条件下反应,生成氯气有毒,需要尾气吸收,故C错误;
D.氨气密度比空气小,应用向下排空法收集,且不能用浓硫酸干燥,故D错误;
故选B.
点评 本题考查气体的制备和收集,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握物质的性质,根据性质判断装置的要求,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
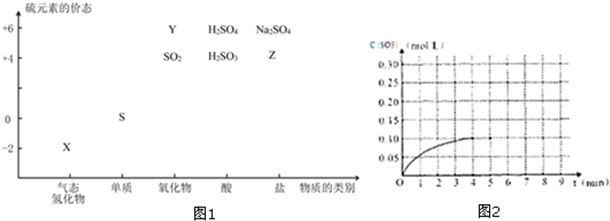
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
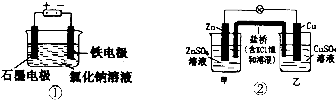
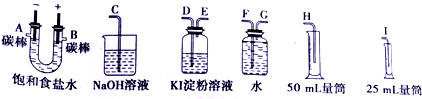
| A. | 装罝①两极均有气泡产生,滴人酚酞溶液后,石墨电极附近溶液变红 | |
| B. | 装置①电解一段时间,加人盐酸溶液可使电解质溶液恢复原状 | |
| C. | 装置②盐桥中的K+向乙池移动 | |
| D. | 装置②反应一段时间后,乙池中溶液的pH变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯的结构简式: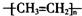 | B. | CH4分子的填充(或比例)模型: | ||
| C. | 乙醇的分子式:CH3CH2OH | D. | 8个中子的碳原子的核素符号:12C |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
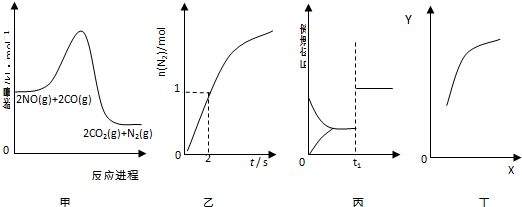
| A. | 由图象甲可知,该反应正反应为放热反应 | |
| B. | 由图象乙可知,0~2s内平均速率V(CO)=1mol•L-1•s-1 | |
| C. | 由图象丙可知,t1时改变的条件可能为增大压强 | |
| D. | 由图象丁中,若X为c(CO),则纵坐标Y可能为NO的转化率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com