
【题目】下列实验与图象不对应的是
选项 | A | B | C | D |
实验 | 向NH4C1溶液中加入过量Na2O2固体 | 向稀硝酸溶液中加入过量的铁粉 | 明矾溶液中逐滴加Ba(OH)2溶液至过量 | 向含等物质的量的NaOH和Na2CO3的混合溶液中滴加过量的稀盐酸 |
图象 |
|
|
|
|
A.AB.BC.CD.D
【答案】D
【解析】
A.向NH4C1溶液中加入过量Na2O2固体,先是Na2O2固体与水反应放出氧气,然后生成的氢氧化钠与氯化铵反应又放出氨气,图象曲线与实际相符,故A正确;
B.在稀硝酸溶液中加入铁粉,先生成Fe3+,当Fe3+的浓度达到最大值时,再加铁粉生成Fe2+,Fe3+的浓度减小,图象符合,故B正确;
C.明矾溶液中逐滴加Ba(OH)2溶液至过量:先生成BaSO4和Al(OH)3,再加入Ba(OH)2生成BaSO4的同时Al(OH)3溶解(此时生成沉淀的速度比前面减小),最后Al(OH)3溶解完,只剩余BaSO4沉淀,产生沉淀先快,再慢,最后不变,C与图象相符,故C正确;
D.设NaOH和Na2CO3的物质的量为nmol,nmolNaOH优先反应消耗nmolHCl,然后Na2CO3与nmolHCl反应生成nmolNaHCO3,最后nmolNaHCO3与nmolHCl生成二氧化碳,则生成二氧化碳气体前后消耗HCl溶液体积之比为2:1,图象中比值为3:1,与实际情况不符,故D错误;
故答案为D。


科目:高中化学 来源: 题型:
【题目】旧键断裂重组新键是有机反应的特点。如图是乙醇的结构式,乙醇在下列反应中化学键的断裂方式不正确的是( )
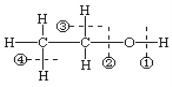
A.与金属钠反应:①B.与乙酸进行酯化:②
C.催化氧化:①③D.实验室制取乙烯:②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(发现问题)研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液。
(实验探究)在体积相同盛满CO2的两集气瓶中,分别加入等体积的饱和石灰水和浓NaOH溶液。实验装置和现象如图所示。请你一起参与。
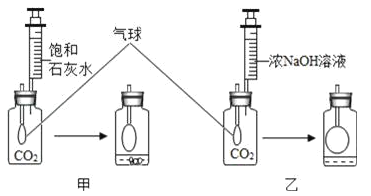
(现象结论)甲装置中产生该实验现象的化学方程式为______________________。解释通常用石灰水而不用NaOH溶液检验CO2的原因________________________________________________;乙装置中的实验现象是___________________________。吸收CO2较多的装置是__________________。
(计算验证)另一位同学小李通过计算发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH。因此,他认为通过吸收CO2应该用饱和石灰水。
(思考评价)请你对小李同学的结论进行评价:________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常以铜铁矿(主要成分为CuO和Fe3O4,还含少量SiO2等杂质)为原料,冶炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要流程如下
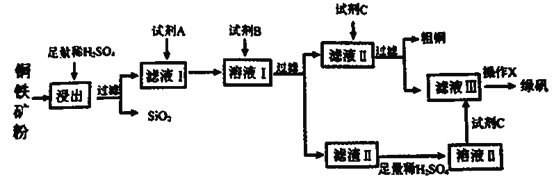
已知:滤渣II的主要成分为Fe(OH)3。请回答下列问题:
(1)如何提高黄铜矿的浸出率___________、___________?(至少答两种方法)
(2)试剂A为___________,其反应的离子方程式为_____________。
(3)试剂B不可能是
A.NH3·H2O B.CuO C.NaOH D.Cu2(OH)2CO3
(4)溶液II中溶质的成分为_______________。
(5)操作X的步骤是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(s)+3B(g)![]() 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
A.v(C)=0.02mol·(L·s)-1B.v(B)=0.06mol·(L·min)-1
C.v(A)=1.5mol·(L·min)-1D.v(D)=0.01mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是三种气态物质,在一定温度下其变化符合下图。下列说法一定正确的是( )
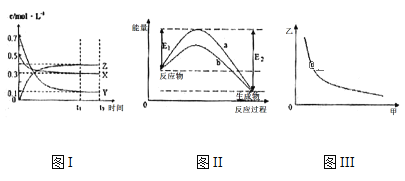
A.该反应的热化学方程式为X(g) +3Y(g) 2Z(g) △H= -(E2-E1)kJ
B.若图III中甲表示压强,乙表示Z的含量,则其变化符合图III中曲线
C.该温度下,反应的平衡常数数值约为533,若升高温度,该反应的平衡常数减小,Y的转化率降低
D.图II中曲线b是加入催化剂时的能量变化曲线,曲线a是没有加入催化剂时的能量变化曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年6月6日,工信部正式向四大运营商颁发了5G商用牌照,揭示了我国5G元年的起点。通信用磷酸铁锂电池其有体积小、重量轻、高温性能突出、可高倍率充放电、绿色环保等众多优点。磷酸铁锂电池是以磷酸铁锂为正极材料的一种锂离子二次电池,放电时,正极反应式为M1-xFexPO4+e-+Li+=LiM1-x FexPO4,其原理如图所示,下列说法正确的是( )
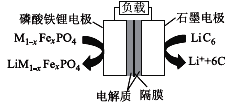
A.放电时,电流由石墨电极流向磷酸铁锂电极
B.电池总反应为M1-xFexPO4+LiC6![]() Li M1-xFexPO4+6C
Li M1-xFexPO4+6C
C.放电时,负极反应式为LiC6-e-=Li++6C
D.充电时,Li+移向磷酸铁锂电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ca3N2是重要的化学试剂,易潮解、被氧化,实验室用N2和金属钙在加热条件下制备Ca3N2的装置如图所示(已知:钙能在CO2中燃烧)。请回答下列问题:
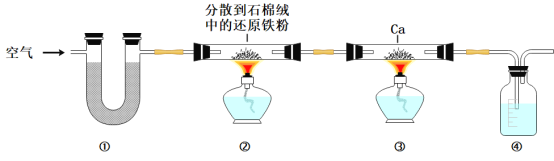
(1)Ca3N2中所含化学键的类型为____________。
A.离子键 B.共价键 C.氢键
(2)装置①中的U型管中的物质为___________,其作用为________________。
(3)装置②的作用为___________________________。
(4)组装好仪器,装入药品,通入空气后,应先点燃____________处酒精灯,再点燃另一个酒精灯。
(5)写出Ca3N2潮解时的化学方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明:H2O2具有立体结构,两个氢原子像在一本半展开的书的两页纸上,两页纸面的夹角为94°,氧原子在书的夹缝上,O—H键与O—O键之间的夹角为97°。下列说法不正确的是( )
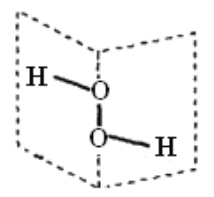
A. H2O2分子中既含极性键,又含非极性键
B. H2O2为极性分子
C. H2O2分子中的两个O原子均是sp3杂化
D. H2O2分子中既有σ键,又有π键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com