

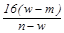 (2分)
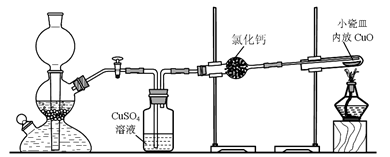
(2分)  mol,CuO中Cu的质量为(w-m)g,其物质的量为
mol,CuO中Cu的质量为(w-m)g,其物质的量为 mol,故可以求其摩尔质量,从而得出相对原子质量。
mol,故可以求其摩尔质量,从而得出相对原子质量。

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源:不详 题型:填空题

| 序号 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| 甲 | 浓硫酸 | Na2SO3 | ① | ② |
| 乙 | 浓硝酸 | Cu | ③ | NaOH |
| 丙 | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
 MnCl2+ Cl2↑+2H2O,在该反应中每生成22.4L(标准状况下)氯气,被氧化HCl的物质的量为__________,转移电子的物质的量为________;d装置中发生反应的离子方程式为_________________。实验室还可以用高锰酸钾和浓盐酸反应制取氯气,完成并配平该反应的离子方程式:
MnCl2+ Cl2↑+2H2O,在该反应中每生成22.4L(标准状况下)氯气,被氧化HCl的物质的量为__________,转移电子的物质的量为________;d装置中发生反应的离子方程式为_________________。实验室还可以用高锰酸钾和浓盐酸反应制取氯气,完成并配平该反应的离子方程式: ____ Mn2+ + ____ Cl2↑+ ____ _________
____ Mn2+ + ____ Cl2↑+ ____ _________查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
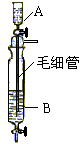
| A.A中装浓硫酸,B中装浓盐酸 |
| B.A中装浓盐酸,B中装浓硫酸 |
| C.A中装氢氧化钠浓溶液,B中装浓氨水 |
| D.A中装浓氨水,B中装氢氧化钠浓溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
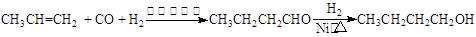
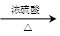 CO↑+H2O,并设计出原料气的制备装置(如下图)
CO↑+H2O,并设计出原料气的制备装置(如下图)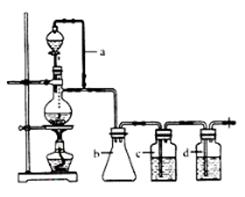
 RCH(OH)SO3Na↓;②沸点:乙醚34℃,
RCH(OH)SO3Na↓;②沸点:乙醚34℃,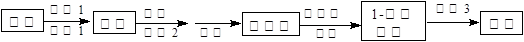
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
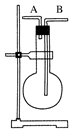
| A.烧瓶是干燥的,由A进气收集①③⑤ |
| B.烧瓶是干燥的,由B进气收集②④⑥⑦⑧ |
| C.在烧瓶中充满水,由A进气收集①③⑤⑦ |
| D.在烧瓶中充满水,由B进气收集⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
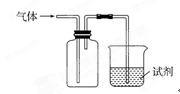
| 选项 | 气体 | 试剂 | 现象 | 结论 |
| A. | NO | 紫色石蕊试液 | 溶液变红 | NO与水反应生成硝酸 |
| B. | C2H4 | 溴水 | 溶液褪色 | 乙烯能与溴发生加成反应 |
| C. | SO2 | 酸性KMnO4溶液 | 溶液褪色 | SO2有还原性 |
| D. | NH3 | MgCl2溶液 | 产生白色沉淀 | NH3有碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
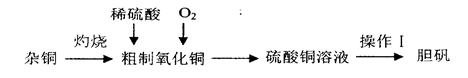
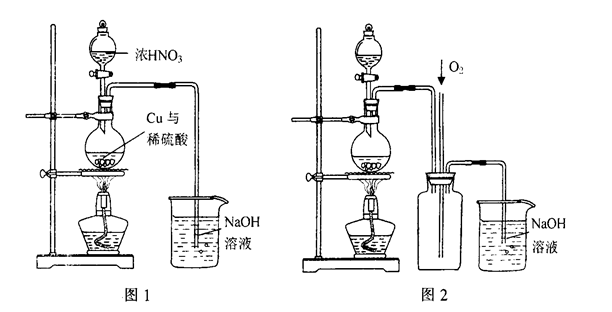
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
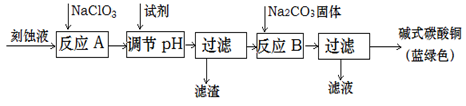
| 物 质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
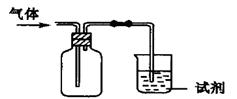
| 选项 | 气体 | 试剂 | 现象 | 结论 |
| A | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | 氯水有酸性和漂白性 |
| B | NH3 | 水 | 无明显现象 | NH3能溶于水 |
| C | X | 澄清石灰水 | 溶液变浑浊 | 气体可能是CO2 |
| D | SO2 | 酸性KMnO4(aq) | 溶液褪色 | SO2有漂白性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com