
”¾ĢāÄæ”æŅŃÖŖĻĀĮŠČČ»Æѧ·½³ĢŹ½£ŗ
¢Ł2H2£Øg£©+O2£Øg£©=2H2O£Øl£©¦¤H=©570 kJ![]()
¢Ś2H2O£Øg£©=2H2£Øg£©+O2£Øg£©¦¤H=+483.6kJ![]()
¢Ū2C£Øs£©+O2£Øg£©=2CO£Øg£©¦¤H=©220.8 kJ![]()
¢ÜC£Øs£©+O2£Øg£©=CO2£Øg£©¦¤H=©393.5 kJ![]()
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÉĻŹö·“Ó¦ÖŠŹōÓŚĪüČČ·“Ó¦µÄŹĒ_______£ØĢīŠ“ŠņŗÅ£©”£
£Ø2£©H2µÄČ¼ÉÕČČĪŖ________”£
£Ø3£©Č¼ÉÕ10 g H2Éś³ÉŅŗĢ¬Ė®£¬·Å³öµÄČČĮæĪŖ________”£
£Ø4£©COµÄČ¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ______________________”£
£Ø5£©H2O£Øl£©=H2O£Øg£©¦¤H=__________”£
”¾“š°ø”æ¢Ś 285 kJmol-1 1 425 kJ CO£Øg£©+![]() O2£Øg£©=CO2£Øg£©¦¤H=©283.1 kJmol-1 +43.2 kJmol-1
O2£Øg£©=CO2£Øg£©¦¤H=©283.1 kJmol-1 +43.2 kJmol-1
”¾½āĪö”æ
£Ø1£©ģŹ±ä“óÓŚ0µÄĪŖĪüČČ·“Ó¦£»
£Ø2£©Č¼ÉÕČČŹĒ1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļŹ±·Å³öµÄČČĮ棻
£Ø3£©øł¾ŻČČ»Æѧ·½³ĢŹ½¼ĘĖć£»
£Ø4£©øĒĖ¹¶ØĀɵÄÓ¦ÓĆ£»
£Ø5£©øĒĖ¹¶ØĀɵÄÓ¦ÓĆ”£
£Ø1£©ÉĻŹö·“Ó¦ÖŠÖ»ÓŠ¢ŚµÄģŹ±ä“óÓŚĮć£¬ŹōÓŚĪüČČ·“Ó¦£»
ÕżČ·“š°ø£ŗ¢Ś”£
£Ø2£©2H2£Øg£©+O2£Øg£©=2H2O£Øl£©¦¤H=©570 kJ”¤mol-1£¬øł¾ŻČ¼ÉÕČȵĶØŅå£¬Č¼ÉÕČČĪŖ570 kJ”¤mol-1/2=285kJ”¤mol-1£»
ÕżČ·“š°ø£ŗ285kJ”¤mol-1”£
£Ø3£©n£ØH2£©=![]() =5mol£¬øł¾ŻČČ»Æѧ·½³ĢŹ½£ŗ
=5mol£¬øł¾ŻČČ»Æѧ·½³ĢŹ½£ŗ
2H2£Øg£©+O2£Øg£©=2H2O£Øl£©¦¤H=©570 kJ![]()
2mol 570kJ
5mol Q
Q=![]() =1425 kJ £¬Č¼ÉÕ10 g H2Éś³ÉŅŗĢ¬Ė®£¬·Å³öµÄČČĮæĪŖ1425 kJ£»
=1425 kJ £¬Č¼ÉÕ10 g H2Éś³ÉŅŗĢ¬Ė®£¬·Å³öµÄČČĮæĪŖ1425 kJ£»
ÕżČ·“š°ø£ŗ1425 kJ”£
£Ø4£©2C£Øs£©+O2£Øg£©=2CO£Øg£©¦¤H=©220.8kJ”¤mol-1 ¢Ū
C£Øs£©+O2£Øg£©=CO2£Øg£©¦¤H=©393.5kJ”¤mol-1 ¢Ü
øł¾ŻøĒĖ¹¶ØĀÉ¢Ü-¢Ū”Į1/2µĆCO£Øg£©+![]() O2£Øg£©=CO2£Øg£©¦¤H=©283.1 kJmol-1£»
O2£Øg£©=CO2£Øg£©¦¤H=©283.1 kJmol-1£»
ÕżČ·“š°ø£ŗCO£Øg£©+![]() O2£Øg£©=CO2£Øg£©¦¤H=©283.1 kJmol-1”£
O2£Øg£©=CO2£Øg£©¦¤H=©283.1 kJmol-1”£
£Ø5£©2H2£Øg£©+O2£Øg£©=2H2O£Øl£©¦¤H=©570 kJ”¤mol-1 ¢Ł
2H2O£Øg£©=2H2£Øg£©+O2£Øg£©¦¤H=+483.6 kJ”¤mol-1 ¢Ś
øł¾ŻøĒĖ¹¶ØĀɣآŁ+ ¢Ś£©/2µĆ£¬H2O£Øg£©=H2O£Øl£©¦¤H=-43.2 kJmol-1£¬ŌņH2O£Øl£©=H2O£Øg£©¦¤H=+43.2 kJmol-1£»
ÕżČ·“š°ø£ŗ+43.2 kJmol-1”£


 æŚĖćÄÜŹÖĻµĮŠ“š°ø
æŚĖćÄÜŹÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀ£¬½«NO2 ÓėSO2 ŅŌĢå»ż±Č1:2 ÖĆÓŚŗćČŻĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗ ![]() ”£ĻĀĮŠÄÜĖµĆ÷øĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŹĒ
”£ĻĀĮŠÄÜĖµĆ÷øĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŹĒ
A. v(SO3 ) = v(NO2 ) B. »ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä
C. »ģŗĻĘųĢåµÄŃÕÉ«±£³Ö²»±ä D. ĆæĻūŗÄ1 mol SO3 µÄĶ¬Ź±Éś³É1 mol NO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°×Ķ·ĪĢĖŲ¾ßÓŠĻŌÖųµÄæ¹¾ś×÷ÓĆ£¬ĘäŗĻ³ÉĀ·ĻßČēĶ¼ĖłŹ¾£ŗ
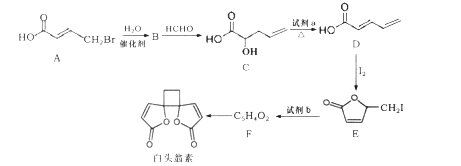
ŅŃÖŖ£ŗ
¢ŁRCH2Br![]() RCH=CHR”Æ
RCH=CHRӮ
¢Ś2RCH=CHR”Æ![]()
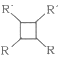
£ØŅŌÉĻR”¢R”Æ“ś±ķĒā”¢Ķ黳£©
(1)°×Ķ·ĪĢĖŲµÄ·Ö×ÓŹ½ĪŖ____”£
(2)ŹŌ¼ĮaĪŖ______£¬E”śFµÄ·“Ó¦ĄąŠĶĪŖ________”£
(3)FµÄ½į¹¹¼ņŹ½ĪŖ_________”£
(4)CÖŠŗ¬ÓŠµÄ¹ŁÄÜĶÅĆū³ĘĪŖ________”£
(5) A”śB·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_________”£
(6)FÓė×ćĮæĒāĘų¼Ó³ÉµĆµ½G£¬GÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬ĘäÖŠŹōÓŚĮ“דōČĖįĄąÓŠ____ÖÖ”£
(7)ŅŌŅŅĻ©ĪŖĘšŹ¼ŌĮĻ£¬Ń”ÓƱŲŅŖµÄĪŽ»śŹŌ¼ĮŗĻ³É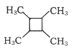 µÄĀ·ĻßĪŖ____£ØÓĆ½į¹¹¼ņŹ½±ķŹ¾ÓŠ»śĪļ£¬ÓĆ¼żĶ·±ķŹ¾×Ŗ»Æ¹ŲĻµ£¬¼żĶ·ÉĻ×¢Ć÷ŹŌ¼ĮŗĶ·“Ó¦Ģõ¼ž£©”£
µÄĀ·ĻßĪŖ____£ØÓĆ½į¹¹¼ņŹ½±ķŹ¾ÓŠ»śĪļ£¬ÓĆ¼żĶ·±ķŹ¾×Ŗ»Æ¹ŲĻµ£¬¼żĶ·ÉĻ×¢Ć÷ŹŌ¼ĮŗĶ·“Ó¦Ģõ¼ž£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĆń¼äŅÕŹõŹĒĄĶ¶ÆČĖĆńÖĒ»ŪµÄ½į¾§£¬ĻĀĮŠÖŠ¹ś“«Ķ³Ćń¼äŅÕŹõŌŚ±ķŃŻ¹ż³ĢÖŠÉę¼°»Æѧ±ä»ÆµÄŹĒ
A | B | C | D |
“ĢŠå | “ņŹ÷»Ø | ¼ōÖ½ | Öƽõ |
|
|
|
|
ÓĆÕėĻßŌŚÖÆĪļÉĻ ŠåÖĘĶ¼°ø | ½«ČŪ»ÆµÄĢśĖ®ĘĆĻņ æÕÖŠ£¬±Å½¦³ö»š»Ø | ÓĆ¼ōµ¶»ņæĢµ¶ŌŚÖ½ÉĻ¼ōæĢ»ØĪĘ | ÓĆĢį»Ø»śÖƳöĶ¼°ø |
A. AB. BC. CD. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌCO2ŗĶNa2O2ĪŖŌĮĻ£¬ÖĘČ”“æ¾»øÉŌļµÄO2£¬ŹµŃé×°ÖĆČēĻĀ£ŗ

ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. ×°ÖĆ¢ŚÖŠŹŌ¼ĮæÉŅŌŹĒNaOHČÜŅŗ
B. ×°ÖĆ¢ŪµÄ×÷ÓĆŹĒøÉŌļO2
C. ŹÕ¼ÆŃõĘųӦєŌń×°ÖĆa
D. ×°ÖĆ¢Ś”¢¢ŪÖ®¼äÓ¦Ōö¼ÓŹ¢³ĪĒåŹÆ»ŅĖ®µÄĻ“ĘųĘæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪĀ¶ČĻĀ,Ģå»żŅ»¶ØµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠČēĻĀæÉÄę·“Ó¦:X(g)+Y(g)![]() Z(g)+W(s)””¦¤H>0”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ(””””)
Z(g)+W(s)””¦¤H>0”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ(””””)
A. ¼ÓČėÉŁĮæW,Äę·“Ó¦ĖŁĀŹŌö“ó,Õż·“Ó¦ĖŁĀŹ¼õŠ” B. ÉżøßĪĀ¶Č,Ę½ŗāÄęĻņŅʶÆ
C. µ±ČŻĘ÷ÖŠĘųĢåŃ¹Ēæ²»±äŹ±,·“Ó¦“ļµ½Ę½ŗā D. ·“Ó¦Ę½ŗāŗó¼ÓČėX,ÉĻŹö·“Ó¦µÄ¦¤HŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒŌŖĖŲÖÜĘŚ±ķ¶ĢÖÜĘŚµÄŅ»²æ·Ö£¬ČōAŌ×Ó×īĶā²ćµÄµē×ÓŹż±Č“ĪĶā²ćµÄµē×ÓŹżÉŁ3£¬ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(””””)

A. DÓėC²»ÄÜŠĪ³É»ÆŗĻĪļ
B. DµÄ×īøßÕż¼ŪÓėBµÄ×īøßÕż¼ŪĻąµČ
C. A”¢B”¢CµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĖįŠŌĒæČõµÄ¹ŲĻµŹĒC>B>A
D. DŌŖĖŲ×īøßÕż¼ŪŗĶ×īµĶøŗ¼ŪµÄ¾ų¶ŌÖµµÄ“śŹżŗĶµČÓŚ8
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»¶ØĢõ¼žĻĀ£¬¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ·“Ó¦£ŗ2NO2(g)![]() O2(g)£«2NO(g)””¦¤H£¾0£¬“ļµ½Ę½ŗā”£µ±øıäĘäÖŠŅ»øöĢõ¼žXŹ±£¬YĖęXµÄ±ä»Æ·ūŗĻĶ¼ÖŠĒśĻߵďĒ
O2(g)£«2NO(g)””¦¤H£¾0£¬“ļµ½Ę½ŗā”£µ±øıäĘäÖŠŅ»øöĢõ¼žXŹ±£¬YĖęXµÄ±ä»Æ·ūŗĻĶ¼ÖŠĒśĻߵďĒ

A. µ±X±ķŹ¾ĪĀ¶ČŹ±£¬Y±ķŹ¾O2µÄĪļÖŹµÄĮæ
B. µ±X±ķŹ¾Ń¹ĒæŹ±£¬Y±ķŹ¾NO2µÄ×Ŗ»ÆĀŹ
C. µ±X±ķŹ¾·“Ó¦Ź±¼äŹ±£¬Y±ķŹ¾»ģŗĻĘųĢåµÄĆܶČ
D. µ±X±ķŹ¾NO2µÄĪļÖŹµÄĮæŹ±£¬Y±ķŹ¾O2µÄĪļÖŹµÄĮæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ½”æµČĖĢåÄŚŗ¬ĢśŌŖĖŲ“óŌ¼ 2~3g£¬ČĖĢåÄŚĢśŌŖĖŲŅŌŃĒĢśĄė×ÓŗĶČż¼ŪĢśĄė×ӵĊĪŹ½“ęŌŚ£¬Fe2+Ņ×±»ĪüŹÕ£¬ĖłŅŌøųʶŃŖÕß²¹³äĢśŌŖĖŲŹ±£¬Ó¦²¹³äŗ¬ Fe2+µÄŃĒĢśŃĪ”£”°ĖŁĮ¦·Ę”±£ØÖ÷ŅŖ³É·Ö£ŗēśēźĖįŃĒĢś£¬³Ź°µ»ĘÉ«£©ŹĒŹŠ³”ÉĻŅ»ÖÖ³£¼ūµÄ²¹ĢśŅ©Īļ”£øĆŅ©Ę·²»ČÜÓŚĖ®µ«ÄÜČÜÓŚČĖĢåÖŠµÄĪøĖį”£Ä³Ķ¬Ń§ĪŖĮĖ¼ģ²ā”°ĖŁĮ¦·Ę”±Ņ©Ę¬ÖŠFe2+µÄ“ęŌŚ£¬Éč¼Ę²¢½ųŠŠĮĖČēĻĀŹµŃé£ŗ

(1) ŹŌ¼Į1µÄĆū³ĘŹĒ__________£»ŹŌ¼Į2µÄ»ÆѧŹ½ĪŖ______________”£
(2) ¼ÓČėŠĀÖĘĀČĖ®£¬ČÜŅŗÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ_____________________________”£
(3) ¼ÓČėŹŌ¼Į2 Ź±ČÜŅŗĪŖµŗģÉ«ĖµĆ÷ ”°ĖŁĮ¦·Ę”±ÖŠµÄ Fe2+ŅŃ²æ·ÖŃõ»Æ£¬Ņ»°ćŌŚ·žÓĆ”°ĖŁĮ¦·Ę”±Ź±£¬Ķ¬Ź±·žÓĆĪ¬ÉśĖŲC£¬ĖµĆ÷Ī¬ÉśĖŲC¾ßÓŠ___________ŠŌ”£
(4) ²»½öČÜŅŗÖŠFe2+Ņ×±»Ńõ»Æ³ÉFe3+£¬ČÜŅŗÖŠ°×É«³ĮµķFe(OH)2øüŅ×±»O2Ńõ»Æ£¬ĒėŠ“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½________________________£¬ĻÖĻóĪŖ__________________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com