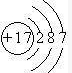
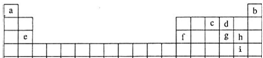
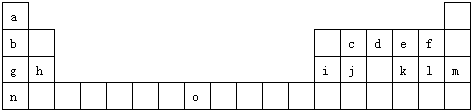
分析:由元素在周期表中的位置可知,A为氢元素,B为Li、C为Be、D为B元素、E为碳元素、F为Na、G为Mg、H为Al、I为Si、J为氮元素、K为氧元素、L为F元素、M为钾元素,
(1)A.同周期自左而右第一电离能呈增大趋势,N元素的2p能级为半满稳定状态,第一电离能高于同周期相邻元素,一般非金属性越强第一电离能越大;
B.同周期自左而右电负性增大;
C.同周期自左而右原子半径减小,同主族自上而下原子半径增大;
D.根据价层电子对互斥理论判断分子空间构型,根据正负电荷重心是否重合判断分子极性;
(2)A.单键为σ键,双键中含有1个σ键、1个π键;
B.根据E成的σ键数目及孤对电子对数确定杂化方式;
C.根据E原子杂化方式,判断分子空间构型,据此判断;
D.根据分子中中间E原子杂化方式,判断3个E原子空间构型;
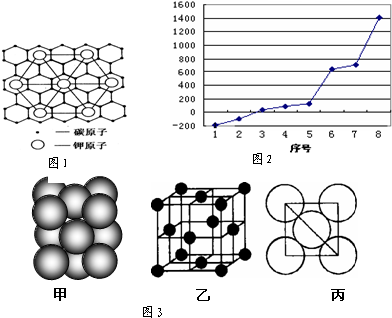
(3)Na晶胞为体心立方,令原子半径为r、晶胞棱长为l,晶胞体对角线为4r,则3l
2=(4r)
2,故l=
,计算晶胞的体积,计算晶胞中Na原子数目、进而计算Na原子总体积,空间利用率=
×100%;
(4)O元素原子有2个电子层,第二电子层含有电子数为6,结合核外电子排布规律书写;
(5)KHF
2晶体属于离子晶体,晶体中H、F原子之间形成极性键;
(6)LiAlH
4是一种络合物,配离子AlH
4-中心Al原子配体为4个H原子,计算Al原子价层电子对数与孤对电子对,确定空间结构.
解答:解:由元素在周期表中的位置可知,A为氢元素,B为Li、C为Be、D为B元素、E为碳元素、F为Na、G为Mg、H为Al、I为Si、J为氮元素、K为氧元素、L为F元素、M为钾元素,
(1)A.同周期自左而右第一电离能呈增大趋势,N元素的2p能级为半满稳定状态,第一电离能高于同周期相邻元素,一般非金属性越强第一电离能越大,故第一电离能N>O>C>H>Li,故A错误;
B.同周期自左而右电负性增大,故电负性B<C<D<E<J,故B错误;
C.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径F>G>H>E,故C正确;
D.B、Si分别与F形成的简单分子分别为BF
3、SiF
4,BF
3分子中B原子价层电子对数=3+
=3、不含孤对电子,故其为平面正三角形,分子中正负电荷重心重合,为非极性分子;SiF
4分子中Si原子价层电子对数=4、不含孤对电子,故其为平面正三角形,分子中正负电荷重心重合,为非极性分子,故D正确,
故答案为:CD;
(2)A
2E=E=EA
2分子为H
2C=C=CH
2,
A.单键为σ键,双键中含有1个σ键、1个π键,故H
2C=C=CH
2分子中有6个σ键和2个π键,故A正确;
B.H
2C=C=CH
2分子中中间C原子成2个σ键、不含孤对电子,杂化轨道数目为2,采取sp杂化,两端C原子都成3个σ键、不含孤对电子,杂化轨道数目为3,采取sp
2杂化,三个碳原子杂化方式不同,故B错误;
C.H
2C=C=CH
2分子中中间C原子成2个σ键、不含孤对电子,杂化轨道数目为2,采取sp杂化,3个碳原子处于同一直线;两端C原子都成3个σ键、不含孤对电子,杂化轨道数目为3,采取sp
2杂化,为平面三角形结构,故该分子为平面结构,所有原子处于同一平面,故C错误;
D.H
2C=C=CH
2分子中中间C原子成2个σ键、不含孤对电子,杂化轨道数目为2,采取sp杂化,3个碳原子处于同一直线,故D正确,
故答案为:BC;
(3)Na晶胞为体心立方,令原子半径为r、晶胞棱长为l,晶胞体对角线为4r,则3l
2=(4r)
2,故l=
,晶胞的体积=(
)
3=
,晶胞中Na原子数目=1+8×
=2、晶胞中Na原子总体积=2×
πr
3,故晶胞空间利用率=
×100%≈68%,
故答案为:68%;
(4)O元素原子有2个电子层,第二电子层含有电子数为6,故原子基态时的价层电子排布式为2s
22p
4,
故答案为:2s
22p
4;
(5)KHF
2晶体属于离子晶体,含有离子键,晶体中H、F原子之间形成极性键,
故答案为:①②;
(6)LiAlH
4是一种络合物,配离子AlH
4-中心Al原子配体为4个H原子,Al原子价层电子对数=4+
=4、不含孤对电子,故AlH
4-为正四面体结构,
故答案为:4;正四面体.

 它的空间利用率为
它的空间利用率为

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案