
��10�֣�ij��ѧʵ��С����г�������һƿijƷ��ʳ�ð״ף���Ҫ�Ǵ����ˮ��Һ������ʵ���ұ�NaOH��Һ������еζ��Բⶨ����ȷŨ�ȣ���ȫ��Ӧʱ������ҺpH����Ϊ9 ���±���4�ֳ���ָʾ���ı�ɫ��Χ��
ָʾ�� | ʯ�� | ���� | ���� | ��̪ |
��ɫ��Χ��pH�� | 5.0��8.0 | 3.1��4.4 | 4.4��6.2 | 8.2��10.0 |
��1����ʵ��Ӧѡ�� ��ָʾ����
��2����ͼ��ʾ50 mL�ζ�����Һ���λ�ã���A��C�̶ȼ����1mL��A���Ŀ̶�Ϊ25���ζ�����Һ�����ӦΪ mL����Ӧ��ζ��յ�ʱ������Ϊ ��
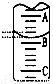
��3��Ϊ��Сʵ������ͬѧһ������������ʵ�飬����ÿ����ȡ�״������ΪV mL��NaOH��ҺŨ��Ϊc mo1/L������ʵ������¼���£�
ʵ����� | ��һ�� | �ڶ��� | ������ |
����NaOH��Һ���/mL | 26.02 | 25.35 | 25.30 |
���ϱ����Կ�������һ��ʵ���м�¼����NaOH��Һ��������Զ��ں����Σ���ԭ������� ��
A��ʵ�����ʱ�����ӿ̶��߶�ȡ�ζ��յ�ʱNaOH��Һ�������
B���ζ�ǰ�ζ��ܼ��������ݣ��ζ��������첿�ֳ�����Һ��
C��ʢװ�״���Һ�ĵζ���������ˮϴ����δ�ð״���Һ��ϴ��
D����ƿԤ����ʳ�ð״���ϴ����
E���μ�NaOH��Һʱ��δ������տ�����Һ��ɫ������ֹͣ�ζ���
��4�������������ݣ�д������ð״��д�������ʵ���Ũ�ȵı���ʽ(���ػ���)��
c�� mol/L��
����10�֣�
��1����̪��2�֣�
��2��25.40 ��2�֣� ��Һ����ɫ��Ϊ�ۺ�ɫ���Ұ�����ڲ���ɫ��2�֣�
��3��BD��2�֣�
��4������25.35+25.30��/2��c/V��2�֣�
��������
�����������1��ʳ���еĴ��������ᣬ����������ǿ����Եζ������Һ�ʼ��ԣ�����ѡ���̪��ָʾ����
��2��A��C�̶ȼ����1mL��ÿһС����0.1ml���ζ��ܵĶ�����ȷ��0.01mL��������ȷ������25.40mL����̪�����ɫ��������Һ��ʼ��ɫ���ζ��յ�ʱΪ��������Һ�������յ�ʱ����������Һ����ɫ��Ϊdz��ɫ��ۺ�ɫ���Ұ�����ڲ���ɫ��
��3��A��ʵ�����ʱ�����ӿ̶��߶�ȡ�ζ��յ�ʱNaOH��Һ���������ʹ����ƫС����������ҲƫС������B���ζ�ǰ�����ݣ���ʹ������ƫС���ζ�����ʧ��������ȷ������ߵIJ�ֵƫ����ȷ��C��ʢװ�״���Һ�ĵζ���������ˮϴ����δ�ð״���Һ��ϴ���Խ����Ӱ�죬����D����ƿ��ʳ����ϴ��ʹ��������ʵ������࣬�����������Ƶ���������ƫ����ȷ��E���μ�NaOH��Һʱ��δ������տ�����Һ��ɫ������ֹͣ�ζ����ζ��յ㻹δ���ʹ���ƫС������ѡBD��
��4����һ�ε�����������ε��������Դ�������ȥ��һ�ε����ݣ��ú����ε����ݽ��м��㣬�����кͷ�Ӧ��ʵ�ʣ������Ũ��Ϊ����25.35+25.30��/2��c/V��
���㣺�����к͵ζ�ʵ�飬ָʾ�����жϣ���������Ũ�ȵļ���


 Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д� Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�����ij�ص���ѧͬ����ҵ������1�ս̰棩1.1.3���ʵ�״̬ ���ͣ������
��1��0��25 molij����A��������15 g��A����Է�������Ϊ��������������
��2����ͬ�¡�ͬѹ��ͬ����������£�H2������A������֮����1��8��A��Ħ������Ϊ��������������������
��3����25�桢101 kPa�������£�ͬ������CH4��A��������֮����15��8��A��Ħ������Ϊ����������
��4������ͬ�ݻ����ܷ�����A��B����25���£�A�г���ag A���壬B�г���ag CH4���壬A��B�ڵ�ѹǿ֮����4��11��A��Ħ������Ϊ��������������������
��5����ͬ�¡�ͬѹ�£���ͬ�����CH4������A���ܶ�֮��Ϊ1��4��A��Ħ������Ϊ��������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������ʡ�߶����ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��0.05molNaOH����ֱ���뵽����100mlҺ���У���Һ�ĵ����Ի������䣬��Һ���ǣ� ����
A������ˮ�� B��0.5mol������ C��0.5mol������ ��D.0.5mol����ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������������ϸ���ѧ�߶���㿼�Ի�ѧ��B�ࣩ�Ծ��������棩 ���ͣ�ѡ����
����֤�����淴ӦN2 + 3H2 2NH3�Ѵﵽƽ��״̬����
2NH3�Ѵﵽƽ��״̬����
��һ��N��N���ѵ�ͬʱ����3��H��H�����ѣ���һ��N��N�����ѵ�ͬʱ����6��N��H�����ѣ���������������ʱ���������ƽ����Է����������ٸı䣻�ܱ���������������ʱ����ϵѹǿ���ٸı䣻��NH3��N2��H2��������������ٸı䣻���º���ʱ�����������ܶȱ��ֲ��䣻������Ӧ����v(H2) = 0.6 mol/(L��min)���淴Ӧ����v(NH3) = 0.4 mol/(L��min)
A��ȫ�� B���٢ۢܢ� C���ڢۢܢݢ� D���ۢݢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������������ϸ���ѧ�߶���㿼�Ի�ѧ��B�ࣩ�Ծ��������棩 ���ͣ�ѡ����
�������ȷ�Ӧ��˵������ȷ����
A��������ȵķ�Ӧһ�������ȷ�Ӧ B��ֻ�зֽⷴӦ�������ȷ�Ӧ
C��ʹ�ô����ķ�Ӧ�����ȷ�Ӧ D������кͷ�Ӧ���淴Ӧ�����ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������������ϸ���ѧ�߶���㿼�Ի�ѧ��A�ࣩ�Ծ��������棩 ���ͣ�ѡ����
����˵���У���ȷ����(����)
A�������£�pH=5.6��NaHSO3��Һ��c( SO32-)-c( H2SO3)= 10-5.6-10-8.4
B��ͬ��ͬѹ�£���ӦH2(g)��Cl2(g)��2HCl(g)�ڹ��պ͵�ȼ�����µĦ�H��ͬ
C�����ȷ�Ӧֻ���ڼ��������²��ܷ�������ˮ�����Ȳ�����
D�������İ�ˮ�����ᷴӦ������Һ������Ϊ���ԣ�������Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������������ϸ���ѧ�߶���㿼�Ի�ѧ��A�ࣩ�Ծ��������棩 ���ͣ�ѡ����
���и�����������ָ����Һ�У����ܴ����������( )
����ɫ��Һ�У�K+��Na+��CO32����SO42��
��pH=11����Һ�У�Na����Ba2����AlO2����ClO��
��ˮ�������c(H+) =10��12mol��L��1����Һ�У�Mg2+��NH4+��HCO3����S2��
�ܼ���Al�ų�H2����Һ�У�Cu2+��NH4+��Cl����NO3��
����ɫ��Һ�У�K����Na+��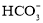 ��
��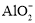 ��������Һ�У�Fe2+��Al3+��NO3����Cl��
��������Һ�У�Fe2+��Al3+��NO3����Cl��
A���٢ڢܡ��� B���٢ڢܢޡ��� C���٢ڡ� ��D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭�ս�����һ������ѧϰ��������ѧ��⣩��ѧ�Ծ��������棩 ���ͣ�ѡ����
ƻ��֭�к���Fe2+����������ϲ����һ�ֲ������ϣ���ե��ƻ��֭�ڿ����л��ɵ���ɫ��Ϊ�ػ�ɫ����ե֭ʱ����ά����C�����Է�ֹ��������������˵��ά����C���У� ��
A����ԭ�� B�������� C������ D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
(8��)��1���£�N2H4���ֳ���������һ�ֿ�ȼ�Ե�Һ�壬���������ȼ�ϡ���֪��101kPaʱ��32��0gN2H4����������ȫȼ�����ɵ������ų�����624kJ��25��ʱ����N2H4��ȼ���Ȼ�ѧ����ʽ�� ��
��2���¡�����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%~30%��KOH��Һ��
�¡�����ȼ�ϵ�طŵ�ʱ�������ĵ缫��Ӧʽ�� ��
��3����ƿ�����õ��һ��ΪǦ���أ�����һ�ֵ��͵Ŀɳ���أ�����ܷ�ӦʽΪ��Pb+PbO2+4H++2SO42- 2PbSO4+2H2O�����ʱ��������Ӧʽ�� �ô�װ�õ��ˮ����ˮ��D2O����ɵĻ��Һ�����缫����Pt����ͨ��һ��ʱ������������ռ���33��6 L����״�������壬������Ϊ18.5 g������������Hԭ�Ӻ�Dԭ�Ӹ���֮�ȣ�
2PbSO4+2H2O�����ʱ��������Ӧʽ�� �ô�װ�õ��ˮ����ˮ��D2O����ɵĻ��Һ�����缫����Pt����ͨ��һ��ʱ������������ռ���33��6 L����״�������壬������Ϊ18.5 g������������Hԭ�Ӻ�Dԭ�Ӹ���֮�ȣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com