
| A.C+CO2=2CO |
| B.Ba(OH)2?8H2O+2NH4Cl=BaCl2+2NH3?H2O+8H2O |
| C.CaC2+2H2O=Ca(OH)2+C2H2 |
| D.CH4+2O2=CO2+2H2O |
科目:高中化学 来源:不详 题型:单选题
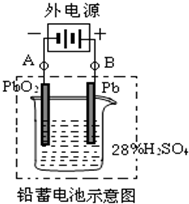
| A.锌片是正极,铜片上有气泡产生 | B.电流方向是从锌片流向铜片 |
| C.溶液中H2SO4的物质的量减少 | D.电解液的pH保持不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,
,查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

| 1 |
| 5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.汽车尾气的净化反应2NO+2CO 2CO2+N2△H<0,则该反应一定能自发进行 2CO2+N2△H<0,则该反应一定能自发进行 |
| B.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
| C.由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀 |
D.对N2(g)+3H2(g) 2NH3(g),其他条件不变时充入N2,正逆反应速率均增大 2NH3(g),其他条件不变时充入N2,正逆反应速率均增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.对于反应2SO2(g)+O2(g)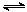 2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 |
| B.电解法精炼铜时,精铜作阳极,粗铜作阴极 |
| C.在硫酸钡悬浊液中加入足量饱和Na2CO3溶液处理,向所得沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
D.CH3COOH溶液加水稀释后,电离程度增大,溶液中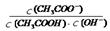 的值不变 的值不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.含1 mol Ba(OH)2的稀溶液和含1 mol H2SO4的稀溶液反应释放热量akJ,则表示该反应中和热的热化学反应方程式为: OH-(aq)+H+(aq)=H2O(l) ?H =" -a" kJ·mol-1 |
| C.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 |
D.对于2HI(g)  H2(g)+I2(g)平衡体系,增大平衡体系的压强可使颜色变深,符合勒夏特列原理解释。 H2(g)+I2(g)平衡体系,增大平衡体系的压强可使颜色变深,符合勒夏特列原理解释。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com