
【题目】已知卤代烃在碱性条件下可以发生如下水解反应:(R 代表烃基)R—X+NaOH![]() R—OH+NaBr。A、B、C、D、E、F、G、H 八种有机化合物有如下转换关系,部分化合物的分子式已给出。
R—OH+NaBr。A、B、C、D、E、F、G、H 八种有机化合物有如下转换关系,部分化合物的分子式已给出。
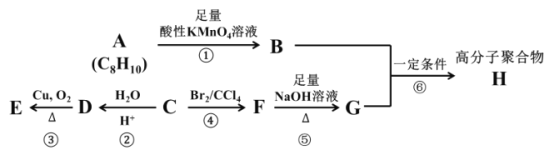
其中,某烃 C 是重要的石油化工产品,其产量可以用来衡量一个国家的石油化工发展水平。化合物 A 属于芳香烃,且苯环上的所有氢原子等效(处于相同的化学环境)。高分子聚合物 H 是工业上重要的聚酯纤维,被大量用于制作矿泉水瓶和衣物纤维。请根据上述信息,回答下列问题:
(1)化合物 A 的结构简式为 _______,A 的二氯代物有____种,A 的分子中最多可能有____个原子共平面。
(2)反应②的反应类型是 _____,化合物 D 中官能团的名称为 ______。
(3)请写出反应③的化学反应方程式______。
(4)请写出反应⑥的化学反应方程式______,并指出该反应的反应类型:_____。
(5)二取代芳香族化合物 I 是化合物 B 的同分异构体,且满足下列条件:
①能发生银镜反应;②不能与NaHCO3 溶液反应生成CO2;③苯环上只含有一种取代基
试写出 I 的任意两种可能的结构简式:______。
【答案】![]() 7 14 加成反应 羟基 2CH3CH2OH+O2
7 14 加成反应 羟基 2CH3CH2OH+O2![]() 2CH3CHO+2H2O n
2CH3CHO+2H2O n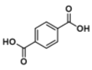 +n
+n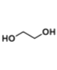
![]()
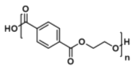 +(2n-1)H2O 缩聚反应
+(2n-1)H2O 缩聚反应 ![]() 、
、 、
、![]()
【解析】
某烃 C 是重要的石油化工产品,其产量可以用来衡量一个国家的石油化工发展水平,则C为乙烯CH2=CH2,C与H2O发生加成反应生成D(CH3CH2OH),D在Cu作用下被O2氧化为E(CH3CHO);C与Br2发生加成反应生成F(BrCH2CH2Br),F在NaOH溶液中发生水解反应生成G(HOCH2CH2OH);化合物 A的分子式为C8H10,其属于芳香烃,且苯环上的所有氢原子等效(处于相同的化学环境),则A为![]() ,被酸性KMnO4溶液氧化生成B(
,被酸性KMnO4溶液氧化生成B(![]() ),B与G发生缩聚反应生成H(
),B与G发生缩聚反应生成H( )。
)。
(1)由以上分析知,化合物 A 的结构简式为![]() ;A 的二氯代物中,两个Cl原子可以取代1个-CH3中的2个H原子,2个-CH3中的2个H原子,1个-CH3中的1个H原子和苯环上的1个H原子(共2种),苯环上的2个H原子(共3种),共有同分异构体7种;A 的分子中,苯环上的12个原子一定共平面,另外,两个-CH3中最多有3个原子共平面,-CH3与苯环共用2个原子,所以最多可能有14个原子共平面;答案为:
;A 的二氯代物中,两个Cl原子可以取代1个-CH3中的2个H原子,2个-CH3中的2个H原子,1个-CH3中的1个H原子和苯环上的1个H原子(共2种),苯环上的2个H原子(共3种),共有同分异构体7种;A 的分子中,苯环上的12个原子一定共平面,另外,两个-CH3中最多有3个原子共平面,-CH3与苯环共用2个原子,所以最多可能有14个原子共平面;答案为:![]() ;7;14;
;7;14;
(2)反应②为CH2=CH2+H2O![]() CH3CH2OH,反应类型是加成反应,化合物 D 为CH3CH2OH,官能团的名称为羟基;答案为:加成反应;羟基;
CH3CH2OH,反应类型是加成反应,化合物 D 为CH3CH2OH,官能团的名称为羟基;答案为:加成反应;羟基;
(3)反应③为CH3CH2OH在Cu作用下被O2氧化为CH3CHO,化学反应方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;答案为:2CH3CH2OH+O2
2CH3CHO+2H2O;答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
(4)反应⑥为HOCH2CH2OH与![]() 发生缩聚反应生成
发生缩聚反应生成 ,化学反应方程式为n
,化学反应方程式为n +n
+n
![]()
 +(2n-1)H2O,反应类型为:缩聚反应;答案为:n
+(2n-1)H2O,反应类型为:缩聚反应;答案为:n +n
+n
![]()
 +(2n-1)H2O;缩聚反应;
+(2n-1)H2O;缩聚反应;
(5)二取代芳香族化合物 I 是![]() 的同分异构体,且满足下列条件:
的同分异构体,且满足下列条件:
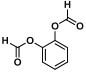
①能发生银镜反应,②不能与NaHCO3 溶液反应生成CO2,③苯环上只含有一种取代基,则表明I中含有2个HCOO-,其可能位于苯环的邻、间、对位置,I 的可能的结构简式为:![]() 、
、 、
、![]() ;答案为:
;答案为:![]() 、
、 、
、![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用价层电子对互斥理论预测H2O和BF3的立体结构,两个结论都正确的是( )
A. 直线形;三角锥形 B. V形;三角锥形
C. 直线形;平面三角形 D. V形;平面正三角形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应mA(g)+nB(g)pC(g)在密闭容器中进行,如图表示反应时间 t时、温度 T 和压强P 与反应混合气体中 C 的体积分数(C%)的关系曲线,由曲线分析,下列判断正确的是
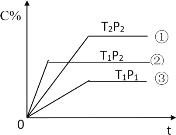
A.T1<T2 P1>P2 m+n<p ΔH>0
B.T1>T2 P1<P2 m+n>p ΔH<0
C.T1<T2 P1>P2 m+n<p ΔH<0
D.T1>T2 P1<P2 m+n>p ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度T℃时,在3个1L的恒容密闭容器中发生:C0(g)+H20(g)= C02(g) + H2(g) △H =-41kJmol-1,其起始时投料的方式、各物质的量及其达平衡过程体系热量的变化入下表所示:
容器编号 | 起始各物质物质的量/mol | 达平衡过程体系热量的变化(均为正值) | |||
C0 | H20(g) | C02 | H2 | ||
① | 1 | 4 | 0 | 0 | 32.8kJ |
② | 8 | 2 | 0 | 0 | Q1 |
③ | 0 | 0 | 1 | 4 | Q2 |
下列说法中正确的是
A. 若经过10s容器①中反应达到平衡,则v(CO)=0.08molL-1s-1
B. 容器②和容器③中热量变化:Q2=Q1=32.8kJ
C. 若加入催化剂,改变了该反应的途径,反应的△H也随之改变
D. 保持相同条件,向平衡后的容器①中再加入0.2molCO(g)和0.8molCO2(g) ,则平衡不发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“温室效应”是全球关注的环境问题之一。C02是目前大气中含量最高的一种温室气体,C02的综合利用是解决温室及能源问题的有效途径。
(1)研究表明C02和H2在催化剂存在下可发生反应生成CH3OH。己知部分反应的热化学方程式如下:CH3OH(g)+![]() O2(g)= CO2(g)+2H2O(g)△H1=akJmol-,H2(g)+
O2(g)= CO2(g)+2H2O(g)△H1=akJmol-,H2(g)+![]() O2(g)=H2O(l)△H2,则CO2(g)+3H2(g)= CH3OH(g)+2H2O(l)△H=___kJmol-。
O2(g)=H2O(l)△H2,则CO2(g)+3H2(g)= CH3OH(g)+2H2O(l)△H=___kJmol-。
(2)C02催化加氢也能合成低碳烯烃:2C02(g)+6H2(g) =C2H4(g)+4H20(g),不同温度下 平衡时的四种气态物质的物质的量如图所示,曲线c表示的物质为____(填化学式)。

(3)C02和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应A: C02(g)+3H2(g) = CH30H(g)+H20(g)
反应B: C02(g)+H2(g)=C0(g)+H20(g)
控制C02和H2初始投料比为1 : 3时,温度对C02平衡转化率及甲醇和CO产率的影响如图所示。
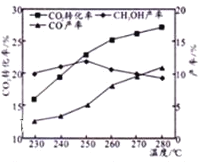
①由图可知温度升高CO的产率上升,其主要原因可能是________。
②由图可知获取CH3OH最适宜的温度是____________。下列措施不能提高C02转化为CH3OH的平衡转化率的有______(填字母)。
A.使用催化剂 B.增大体系压强 C.增大C02和出的初始投料比
(4)在催化剂表面通过施加电压可将溶解在酸性溶液中的二氧化碳直接转化为乙醇,则生成 乙醇的电极反应式为_________。
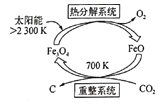
(5)由C02制取C的太阳能工艺如图所示。“热分解系统”发生的反应为 2Fe304 ![]() 6Fe0+02↑。毎分解1mo;Fe304转移电子的物质的量为______;“重整系统”发生反应的化学方程式为_______。
6Fe0+02↑。毎分解1mo;Fe304转移电子的物质的量为______;“重整系统”发生反应的化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应aA(g)+bB(g)cC(g) ΔH<0在等容条件下进行。改变其它反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法不正确的是
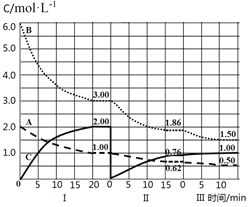
A.反应的化学方程式中,a:b:c=1:3:2
B.第II阶段反应温度小于第III阶段反应温度
C.A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A),最大的是vⅠ(A)
D.由第一次平衡到第二次平衡,采取的措施是从反应体系中移走C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量A、B混合气体发生反应:aA(g)+bB(g)![]() cC(g)。平衡时测得A的浓度为0.5mol/L;保持温度不变,将容器的容积扩大到原来的两倍,再次达到平衡时,测得A的浓度为0.28mol/L。下列有关判断正确的是
cC(g)。平衡时测得A的浓度为0.5mol/L;保持温度不变,将容器的容积扩大到原来的两倍,再次达到平衡时,测得A的浓度为0.28mol/L。下列有关判断正确的是
A. a+b=cB. 该变化使平衡正向移动
C. B的转化率降低D. C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象和解释或结论都正确的是()
选项 | 实验操作 | 现象 | 解释或结论 |
A | 把SO2通入紫色石蕊试液中 | 紫色先变红后褪色 | SO2具有漂白性 |
B | 向AgCl沉淀中清加KI溶液 | 白色沉淀变为黄色 | 溶度积:AgI比AgCl更小 |
C | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变浅 | 反应2NO2 |
D | 把浓硫酸滴到pH试纸上 | 试纸变红 | 浓硫酸具有酸性 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,则下列说法中,正确的是( )
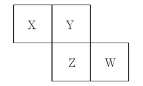
A.原子半径:W>Z>Y>X
B.形成氢化物的稳定性:Z>W
C.常温下:X、Y、Z、W形成的常见单质均为气态
D.W的单质能与水反应,生成一种具有漂白性的物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com