
øõÄÜĀżĀżµŲČÜÓŚĻ”ŃĪĖįµĆµ½Ą¶É«ČÜŅŗ£¬ČōĶØČėæÕĘųŌņČÜŅŗŃÕÉ«±äĀĢ£¬·¢ÉśµÄ·“Ó¦ÓŠ¢ŁCr£«2HCl===CrCl2£«H2”ü£»¢Ś4CrCl2£«4HCl£«O2===4CrCl3£«2H2O£¬ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ(””””)
A£®·“Ó¦¢Ł”¢¢Ś¾łŹōÓŚÖĆ»»·“Ó¦
B£®HClŌŚ·“Ó¦¢Ł”¢¢ŚÖŠ¾ł×öŃõ»Æ¼Į
C£®·“Ó¦¢ŁÖŠHCl±»Ńõ»Æ
D£®ČÜŅŗŃÕÉ«ÓÉĄ¶±äĀĢŹĒŅņĪŖCr2£«·¢ÉśŃõ»Æ·“Ó¦
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠŅ»Ī“ÖŖµÄĪŽÉ«ČÜŅŗ£¬Ö»æÉÄÜŗ¬ÓŠŅŌĻĀĄė×ÓÖŠµÄČōøÉÖÖ£ØŗöĀŌÓÉĖ®µēĄė²śÉśµÄH+”¢OH-£©£ŗH+”¢NH4+”¢K£«”¢Mg2£«”¢Cu2£«”¢Al3+”¢NO3£”¢CO32£”¢SO42££¬ĻÖȔȿ·Ż100mLČÜŅŗ½ųŠŠČēĻĀŹµŃé£ŗ
¢ŁµŚŅ»·Ż¼Ó×ćĮæAgNO3ČÜŅŗŗó£¬ÓŠ°×É«³Įµķ²śÉś”£
¢ŚµŚ¶ž·Ż¼Ó×ćĮæBaCl2ČÜŅŗŗó£¬ÓŠ°×É«³Įµķ²śÉś£¬¾Ļ“µÓ”¢øÉŌļŗ󣬳ĮµķÖŹĮæĪŖ6.99 g”£
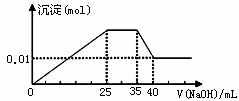
¢ŪµŚČż·ŻÖšµĪµĪ¼ÓNaOHČÜŅŗ£¬²āµĆ³ĮµķÓėNaOHČÜŅŗµÄĢå»ż¹ŲĻµČēĶ¼”£øł¾ŻÉĻŹöŹµŃ飬ŅŌĻĀĶĘ²ā²»ÕżČ·µÄŹĒ
A.ŌČÜŅŗŅ»¶Ø²»“ęŌŚH+”¢Cu2£«”¢CO32£
B.²»ÄÜČ·¶ØŌČÜŅŗŹĒ·ńŗ¬ÓŠK£«”¢NO3£
C. ŹµŃéĖł¼ÓµÄNaOHµÄÅضČĪŖ2mol”¤L£1
D. ŌČÜŅŗČ·¶Øŗ¬Mg2£«”¢Al3£«”¢NH4£«£¬ĒŅn(Mg2£«)n(Al3£«)n( NH4£«)£½112
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŹµŃéŹŅĄļæÉ°“ČēĶ¼ĖłŹ¾µÄ×°ÖĆøÉŌļ”¢“¢“ęĘųĢåR£¬¶ąÓąµÄĘųĢåæÉÓĆĖ®ĪüŹÕ£¬ŌņRŹĒ(””””)
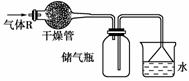
A£®NO2 B£®HCl
C£®CO2 D£®NH3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ėę×ÅČĖĆĒÉś»īÖŹĮæĢįøߣ¬·Ļµē³Ų±ŲŠė½ųŠŠ¼ÆÖŠ“¦ĄķµÄĪŹĢāÓÖ±»Ģįµ½ŅéŹĀČÕ³ĢÉĻ£¬ĘäŹ×ŅŖŌŅņŹĒ(””””)
A£®ĄūÓƵē³ŲĶāæĒµÄ½šŹō²ÄĮĻ
B£®»ŲŹÕĘäÖŠŹÆÄ«µē¼«
C£®·ĄÖ¹µē³ŲÖŠ¹Æ”¢ļÓŗĶĒ¦µČÖŲ½šŹōĄė×Ó¶ŌĖ®ŗĶĶĮČĄµÄĪŪČ¾
D£®²»Ź¹µē³ŲÖŠŠ¹Ā©µÄµē½āŅŗøÆŹ“ĘäĖūĪļĘ·
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĒėÄćÉč¼ĘŅ»øöÄÜÖ¤Ć÷ĢśµÄ½šŹō»ī¶ÆŠŌ±ČĶĒæµÄŹµŃ锣ŅŖĒó£ŗ
¢Ł“Ė·½°øÄܽ«»ÆѧÄÜ×Ŗ»ÆĪŖµēÄÜ£»
¢Ś»ę³öŹµŃé×°ÖĆĶ¼²¢×¢Ć÷ĖłŠčµÄŅ©Ę·£»
 ¢ŪŠ“³öŹµŃé¹ż³ĢÖŠµÄÖ÷ŅŖŹµŃéĻÖĻó”£
¢ŪŠ“³öŹµŃé¹ż³ĢÖŠµÄÖ÷ŅŖŹµŃéĻÖĻó”£
ŹµŃé×°ÖĆ
ŹµŃéĻÖĻó£ŗ______________________________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŹµŃéŹŅÖŠŃøĖŁÖʱøÉŁĮæĀČĘųæÉĄūÓĆČēĻĀ·“Ó¦£ŗ
2KMnO4£«16HCl===2KCl£«2MnCl2£«5Cl2”ü£«8H2O
“Ė·“Ó¦ŌŚ³£ĪĀĻĀ¾ĶæÉŅŌŃøĖŁ½ųŠŠ£¬¶ųĒŅ¶ŌŃĪĖįÅضČŅŖĒó²»øß”£
(1)ŅŃÖŖøßĆĢĖį¼ŲŗĶĀČ»ÆĆĢ¶¼ŹōÓŚæÉČÜŠŌŃĪ£¬Ēė°ŃÉĻŹö»Æѧ·½³ĢŹ½øÄŠ“ĪŖĄė×Ó·½³ĢŹ½£ŗ________________________________________________________________________”£
(2)øĆ·“Ó¦ÖŠ£¬Ńõ»Æ¼ĮŹĒ________£¬»¹Ō¼ĮŹĒ________”£µ±ÓŠ1 molŃõ»Æ¼Į²Ī¼Ó·“Ó¦Ź±£¬±»Ńõ»ÆµÄ»¹Ō¼ĮµÄĪļÖŹµÄĮæŹĒ________£¬²śÉśµÄĀČĘųŌŚ±ź×¼×“æöĻĀµÄĢå»żŌ¼ĪŖ________”£
(3)HClŌŚ“Ė·“Ó¦¹ż³ĢÖŠ±ķĻÖ³öµÄ»ÆѧŠŌÖŹÓŠ________”£
A£®ĖįŠŌ B£®»¹ŌŠŌ
C£®Ńõ»ÆŠŌ D£®»Ó·¢ŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĪļÖŹÖŠ²»ÄÜ×ö»¹Ō¼ĮµÄŹĒ(””””)
A£®H2S B£®Fe2£« C£®Fe3£« D£®SO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
“óĘųÖŠµÄ³ōŃõ²ćæÉŹ¹ČĖĄąŗĶĘäĖūÉśĪļĆāŹÜ×ĻĶāĻßµÄĪ£ŗ¦£¬ČĖĪŖŅņĖŲæÉÄÜŹ¹³ōŃõ²ćŹÜµ½ĘĘ»µ£¬ĻĀĮŠŅņĖŲæÉĘĘ»µ³ōŃõ²ćµÄŹĒ(””””)
A£®SO2µÄÅÅ·Å
B£®ÖĘĄä¼Į·śĀČĢž(ÉĢĘ·Ćū·śĄū°ŗ)µÄŠ¹Ā©
C£®CO2µÄÅÅ·Å
D£®Č¼ĮĻµÄ²»ĶźČ«Č¼ÉÕ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¼×“¼ŹĒŅ»ÖÖŠĀŠĶµÄĘū³µ¶ÆĮ¦Č¼ĮĻ£¬¹¤ŅµÉĻæÉĶعżCO(COµÄ½į¹¹Ź½ĪŖ
C”ŌO)ŗĶH2»ÆŗĻÖʱø¼×“¼£¬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ
¢ŁCO(g)£«2H2(g)====CH3OH(g) ¦¤H1
øĆ·“Ó¦µÄŌĮĻCOŗĶH2±¾Éķ¶¼æÉ×÷ĪŖČ¼ĮĻĢį¹©¶ÆĮ¦£¬ŅŃÖŖÕāĮ½ÖÖĪļÖŹČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½ĪŖ
¢ŚCO(g)£«1/2O2(g)====CO2(g) ¦¤H2£½£283 kJ”¤mol-1
¢ŪH2(g)£«1/2O2(g)====H2O(g) ¦¤H3£½£242 kJ”¤mol-1
¶ĻæŖ1 molijŠ©»Æѧ¼üĖłŠčµÄ×īµĶÄÜĮæŹż¾ŻČēĻĀ±ķ£¬Ēė»Ų“šĻĀ ĮŠĪŹĢā£ŗ
ĮŠĪŹĢā£ŗ

(1)·“Ó¦¢Ł µÄģŹ±ä¦¤H1£½_________”£
µÄģŹ±ä¦¤H1£½_________”£
(2)CH3OH(g)Č¼ ÉÕÉś³ÉCO2(g)ŗĶH2O(g)µÄČČ
ÉÕÉś³ÉCO2(g)ŗĶH2O(g)µÄČČ »Æѧ·½³ĢŹ½ĪŖCH3OH(g)£«3/2O2(g)
»Æѧ·½³ĢŹ½ĪŖCH3OH(g)£«3/2O2(g)
====CO2(g)£«2H2O(g) ¦¤H4£¬øĆ·“Ó¦µÄģŹ±ä¦¤H4=______________________”£
ÓėCOŗĶH2Ļą±Č£¬¼×“¼×÷ĪŖĘū³µ¶ÆĮ¦Č¼ĮĻµÄÓŵćŹĒ_______________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com