
【题目】如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨晶体结构中的某一种的某一部分。
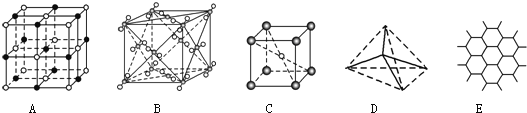
(1)代表金刚石的是________(填字母编号,下同),其中每个碳原子与______个碳原子最近且距离相等;金刚石属于________晶体。
(2)代表石墨的是_______,每个正六边形占有的碳原子数平均为_______个;
(3)代表NaCl的是_______,每个Na+周围与它最近且距离相等的Na+有_______个;
(4)代表CsCl的是_______,它属于_______晶体,每个Cs+与个_______Cl-紧邻;
(5)代表干冰的是_______,它属于_______晶体,每个CO2分子与_______个CO2分子紧邻;
(6)则上述五种物质熔点由高到低的排列顺序为______________(用字母编号回答)。
【答案】(1)D 4 原子
(2)E 2
(3)A 12
(4)C 离子 8
(5)B 分子 12
(6)石墨>金刚石>NaCl>CsCl>干冰
【解析】
试题分析:(1)金刚石是空间网状结构,每个碳原子连接4个碳原子,原子间以共价键相结合,属于原子晶体;
(2)石墨是平面层状结构,其晶体中碳原子呈平面正六边形排列,每个正六边形占有的碳原子数平均=1×![]() ×6=2;
×6=2;
(3)NaCl是离子晶体,其构成微粒是阴阳离子,NaCl晶胞是简单的立方单元,阴阳离子间通过离子键结合,氯离子和钠离子的配位数都是6,每个钠离子周围有6个氯离子,每个钠离子周围与它最接近且距离相等的钠离子数=3×8×![]() =12;
=12;
(4)CsCl是由阴阳离子构成的,属于离子晶体,氯离子和铯离子的配位数是8,故选C;
(5)干冰是分子晶体,CO2分子位于立方体的顶点和面心上,以顶点上的CO2分子为例,与它距离最近的CO2分子分布在与该顶点相连的12个面的面心上,所以图B为干冰晶体;
(6)晶体熔沸点:原子晶体>离子晶体>分子晶体,离子晶体熔沸点与离子半径成正比,与电荷成正比,金刚石是原子晶体、NaCl和CsCl是离子晶体、干冰是分子晶体、石墨是混合型晶体,根据配位数及晶胞结构知,A、B、C、D、E分别是NaCl、干冰、CsCl、金刚石、石墨,钠离子半径小于铯离子半径,石墨中C-C键长小于金刚石中C-C键长,所以这几种晶体熔点高低顺序是石墨>金刚石>NaCl>CsCl>干冰。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】分子式为C3H7Br 的有机物甲在适宜的条件下能发生如下一系列转化:
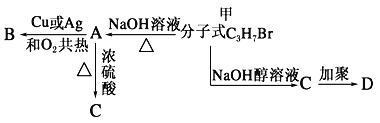
(1)若B能发生银镜反应,试回答下列问题:
①试确定有机物甲的结构简式:___________;
②用化学方程式表示下列转化过程:甲+ NaOH:___________________B+Ag(NH3)2OH:_________________
(2)若B不能发生银镜反应,请回答下列问题:
①试确定A的结构简式______________;
②用化学方程式表示下列转化过程:甲+NaOH![]() ____________________A→B:_____________________C→D:_____________________
____________________A→B:_____________________C→D:_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液。各物质间的转化如下图所示,回答下列各问题(部分生成物未列出):

(1)A的电子式:___________________;
(2)写出甲与C反应的化学方程式:________________________________;
(3)在F和E的混合溶液中用___________试剂(填化学式)检验E中阳离子;
(4)整个转换过程中属于氧化还原反应的有___________个;
(5)写出反应③E与G按物质的量之比2:1的反应的离子方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的Na2CO3和NaHCO3的均匀混合物分成质量不等的三份,分别与50mL相同浓度的盐酸反应,得到气体的质量与固体混合物的质量关系如下表所示:
组 别 | 1 | 2 | 3 |
固体质量/g | 3.80 | 6.20 | 7.20 |
气体质量/g | 1.76 | 2.64 | 2.64 |
(1)上表中_______组数据表明盐酸参加反应后有剩余,理由是______________。
(2)上表中第2组数据中盐酸____________(填“过量”、“适量”、“不足量”)。
(3)通过计算求Na2CO3和NaHCO3的质量分数各为_________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、Y、Z为常见短周期元素,三种元素分属不同周期不同主族,且与X能形成如图结构的化合物。已知W、Y、Z的最外层电子数之和等于X的核外电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是( )
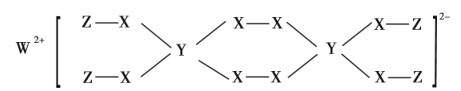
A.对应元素形成的气态氢化物稳定性:Y>X
B.W、X对应的简单离子半径顺序为:X>W
C.Y的氧化物对应水化物为强酸
D.该化合物中各元素均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化硼是一种典型的超硬无机材料,常以BCl3、PH3为原料制备,氮化硼(BN)和磷化硼相似。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,立方相氮化硼是超硬材料,有优异的耐磨性。晶体多种相结构如图所示。
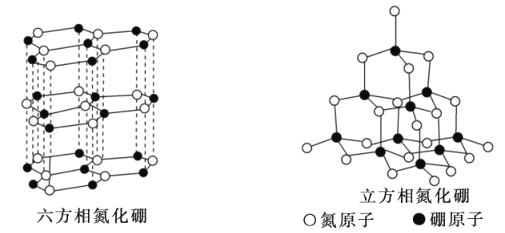
(1)与BCl3分子互为等电子体的一种离子为__(填化学式);预测PH3分子的空间构型为__。
(2)关于氮化硼两种相结构的说法,正确的是__(填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体
(3)六方相氮化硼晶体结构与石墨相似却不导电,原因是__;立方相氮化硼晶体中,硼原子的杂化轨道类型为__。
(4)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1molNH4BF4含有__mol配位键。
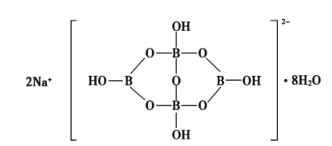
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式可以写作Na2B4O710H2O,实际上它的结构单元是由两个H3BO3和两个[B(OH)4]缩合而成的双六元环,应该写成Na2[B4O5(OH)4]8H2O。其结构如图所示,它的阴离子可通过__(填作用力)相互结合形成链状结构。
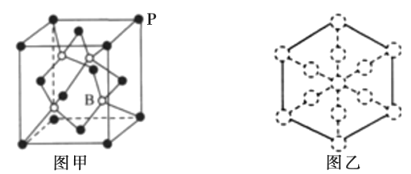
(6)磷化硼晶胞的示意图如图甲所示,其中实心球表示P原子,空心球表示B原子,晶胞中P原子空间堆积方式为__;设阿伏加德罗常数的值为NA,晶胞参数为acm,磷化硼晶体的密度为__gcm-3;若磷化硼晶胞沿着体对角线方向的投影如图乙所示(虚线圆圈表示P原子的投影),请在图乙中用实心圆点画出B原子的投影位置__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. NO2、SO2、BF3、NCl3分子中没有一个分子的原子最外层电子都满足8电子稳定结构
B. P4和CH4都是正四面体分子且键角都为109°28′
C. NH4+的电子式为 ,离子呈平面正方形结构
,离子呈平面正方形结构
D. 用CCl4提取碘水中的碘单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型,据此回答下列问题:

(1)同物质的量的A、B、C、D燃烧,耗氧量最大的是________(填对应字母);同质量的A、B、C、D燃烧,耗氧量最大的是________(填对应字母);
(2)所有原子都在同一平面上的是________(填对应字母);
(3)能使酸性高锰酸钾褪色的是________(填对应字母);
(4)写出F与氢气加成的化学方程式______________________________;
(5)写出C与溴水反应的化学方程式___________________________________;
(6)写出D的实验室制法的化学方程式______________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四个数据都表示合成氨的反应速率,其中速率相等的是( )
①![]() (N2)=0.6mol/(L·min) ②
(N2)=0.6mol/(L·min) ②![]() (NH3)=1.8mol/(L·min)
(NH3)=1.8mol/(L·min)
③![]() (H2)=1.2mol/(L·min) ④
(H2)=1.2mol/(L·min) ④![]() (H2)=0.045mol/(L·s)
(H2)=0.045mol/(L·s)
A. ①②B. ①③C. ③④D. ②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com