
【题目】已知:还原性强弱:I->Fe2+。往100 mL碘化亚铁溶液中缓慢通入3.36 L(标准状况)氯气,反应完成后溶液中有一半的Fe2+被氧化成Fe3+。则原碘化亚铁溶液的物质的量浓度为
A. 1.2 mol·L-1 B. 1.5 mol·L-1 C. 1.0 mol·L-1 D. 1.1 mol·L-1
【答案】A
【解析】已知:还原性强弱:I->Fe2+,往100mL碘化亚铁溶液中缓慢通入3.36L(标准状况)氯气,氯气先氧化碘离子,再氧化亚铁离子,已知氯气的物质的量为 ![]() =0.15mol,发生反应离子方程式为:Cl2+2I-=2Cl-+I2,碘离子完全氧化后,溶液中有
=0.15mol,发生反应离子方程式为:Cl2+2I-=2Cl-+I2,碘离子完全氧化后,溶液中有 ![]() 的Fe2+被氧化成Fe3+,发生反应离子方程式为:Cl2+2Fe2+=2Cl-+Fe3+,设原碘化亚铁溶液的物质的量浓度为cmol/L,则c(I-)=2c(FeI2)=2c,c(Fe2+)=cmol/L,所以与碘离子反应消耗的氯气为n(Cl2)=
的Fe2+被氧化成Fe3+,发生反应离子方程式为:Cl2+2Fe2+=2Cl-+Fe3+,设原碘化亚铁溶液的物质的量浓度为cmol/L,则c(I-)=2c(FeI2)=2c,c(Fe2+)=cmol/L,所以与碘离子反应消耗的氯气为n(Cl2)= ![]() n(I-)=
n(I-)= ![]() cV=0.1cmol,反应完成后溶液中有
cV=0.1cmol,反应完成后溶液中有![]() 的Fe2+被氧化成Fe3+,则与亚铁离子反应消耗的氯气为n(Cl2)=
的Fe2+被氧化成Fe3+,则与亚铁离子反应消耗的氯气为n(Cl2)= ![]() ×
× ![]() n(Fe2+)=
n(Fe2+)= ![]() cV=0.025cmol,所以0.025cmol+0.1cmol=0.15mol,解得:c=1.2mol/L,答案选A。
cV=0.025cmol,所以0.025cmol+0.1cmol=0.15mol,解得:c=1.2mol/L,答案选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】元素性质呈周期性变化的本质是 ( )
A. 元素原子核外电子排布呈周期性变化 B. 元素的相对原子质量依次递增
C. 元素原子半径大小呈周期性变化 D. 元素的最高正化合价呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,错误的是 ( )
A. 化学变化中的能量变化主要是由化学键变化引起的
B. 化学反应中能量变化的大小与反应物的质量多少无关
C. 化学反应必然伴随发生能量变化
D. 能量变化是化学反应的基本特征之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能表示阿伏加德罗常数值的是( )
A. 1 mol金属钠含有的电子数
B. 标准状况下,22.4 L苯所含的分子数
C. 0.012 kg 12 C所含的原子数
D. 1 L 1 mol·L-1硫酸溶液所含的H+数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:4NH3+5O2![]() 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[mol/(L·min)]表示,则正确的关系式是
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[mol/(L·min)]表示,则正确的关系式是
A. 4v(NH3)=5v(O2) B. 5v(O2)=6v(H2O) C. 2v(NH3)=3v(H2O) D. 4v(O2)=5v(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种有机合成中间体,Z是常见的高分子化合物,某研究小组采用如下路线合成X和Z:
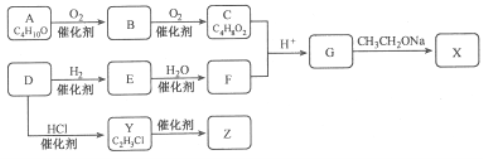
已知:①化合物A的结构中有2个甲基
②RCOOR′+R′′CH2COOR′![]()
![]()
请回答:(1)写出化合物E的结构简式__________,F中官能团的名称是_________。
(2)Y→Z的化学方程式是____________。
(3)G→X的化学方程式是__________,反应类型是___________。
(4)能与NaOH反应的G的同分异构体有_____种
(5)若C中混有B,请用化学方法检验B的存在(要求写出操作、现象和结论)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为单质,B、C、D、E为化合物,它们之间存在如下转化关系:
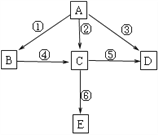
(1)若A为非金属单质,B为镁条在空气中燃烧的产物之一,其与水反应可生成气体C,D为无色气体,在空气中可变成红棕色,C与HCl气体反应生成E时产生大量白烟,则B的电子式为___________,B与盐酸反应的化学方程式为___________________,上述反应中属于氧化还原反应的有________。
(2)若A为生活中常见的金属单质,B为A与盐酸反应的产物,C可通过单质间的化合反应制得,加热蒸干并灼烧C的溶液可得到红棕色的D,将C滴入沸水中可得E的胶体,则由B转化为C的离子方程式为________________,加热蒸干并灼烧C的溶液可得D的原因是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com