(2009?安徽模拟)A、B、C、D、E、F均为短周期元素,原子序数依次增大,A元素原子核内无中子.B元素原子核外最外层电子数是次外层电子数的2倍.C元素是地壳中含量最多的元素.D是短周期元素中金属性最强的元素.E与D元素的质子数之和为27,最外层电子数之差为5.F元素的最高价氧化物的水化物为强酸.
(1)推断B元素在周期表中的位置:第
二
二
周期
ⅣA
ⅣA
族.
(2)写出F元素的电子排布式:
1s22s22p63s23p5
1s22s22p63s23p5
.
(3)C、D元素可形成淡黄色的粉末,其电子式为
,所含化学键为
离子键、非极性共价键
离子键、非极性共价键
.
(4)写出A与C元素形成10电子的微粒:
H2O
H2O
、
H3+O
H3+O
、
OH-
OH-
.
(5)D、E元素形成的正盐的水溶液,阴离子的浓度大小顺序为:(从大到小排列)
c(S2-)>c(OH-)>c(HS-)
c(S2-)>c(OH-)>c(HS-)
.
(6)常温下,1molA元素的单质与C元素的单质化合,放出286kJ的热量.写出反应的热化学方程式:
H2(g)+1/2O2(g)=H2O(l);△H=-286kJ/mol
H2(g)+1/2O2(g)=H2O(l);△H=-286kJ/mol
.

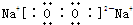
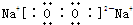
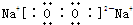 .钠离子与过氧根离子之间形成离子键,过氧根离子中氧原子之间形成1对共用电子对,是非极性共价键.
.钠离子与过氧根离子之间形成离子键,过氧根离子中氧原子之间形成1对共用电子对,是非极性共价键.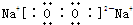 ;离子键、非极性共价键.
;离子键、非极性共价键.
