
下列事实与氢键有关的是( )
|
| A. | HF、HCl、HBr、HI的热稳定性依次减弱 |
|
| B. | 水加热到很高的温度都难以分解 |
|
| C. | CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 |
|
| D. | 水结成冰体积膨胀 |
考点:
氢键的存在对物质性质的影响.
专题:
化学键与晶体结构.
分析:
A.只有HF存在氢键;
B.氢键为分子间作用力,与物质的稳定性无关;
C.都不存在氢键;
D.水中存在氢键,水结成冰体积膨胀.
解答:
解:A.非金属性越强,对应的氢化物越稳定,只有HF存在氢键,但与氢键无关,故A错误;
B.氢键为分子间作用力,与物质的稳定性无关,故B错误;
C.都不存在氢键,影响熔点高低的因素是分子间作用力,故C错误;
D.水中存在氢键,氢键具有方向性,水结成冰体积膨胀,故D正确.
故选D.
点评:
本题考查氢键的知识,题目难度不大,注意氢键只与物质的物理性质有关,与化学性质无关.


科目:高中化学 来源: 题型:
现有A、B、C、D四种元素,它们的质子数依次增多.
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
(1)写出C、D的名称:C钾;碘
(2)A在周期表中的位置
(3)写出B2A3与氢氧化钠溶液反应的离子方程式 .
(4)比较B、C二种元素形成的简单离子半径的大小(用离子符号表示):离子半径: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列操作或发生事故时的处理方法正确的是()
A. 浓硫酸不慎沾在皮肤上,应立即用大量水冲洗,再涂上3%~5%的小苏打溶液
B. 给试管里的液体加热时,试管应与桌面垂直
C. 配制一定物质的量浓度的NaCl溶液时,定容、振荡、摇匀后,发现液面低于刻度线,再加水到刻度线
D. 将pH试纸用蒸馏水润湿后,测定稀盐酸的pH值
查看答案和解析>>
科目:高中化学 来源: 题型:
已知M2O7x﹣+3S2﹣+14H+=2M3++3S↓+7H2O,则M2O7x﹣中的M的化合价为()
A. +2 B. +3 C. +4 D. +6
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组微粒中,都互为等电子体的是( )
|
| A. | CO、NO、NaH、N2 | B. | SO2、NO2+、N3﹣、OCN﹣ |
|
| C. | CO32﹣、NO3﹣、BCl3 | D. | SiF4、SiO44﹣、SO32﹣、PO43﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
碘单质在水溶液中溶解度很小,但在CCl4中溶解度很大,这是因为( )
|
| A. | CCl4与I2分子量相差较小,而H2O与I2分子量相差较大 |
|
| B. | CCl4与I2都是直线型分子,而H2O不是直线型分子 |
|
| C. | CCl4和I2都不含氢元素,而H2O中含有氢元素 |
|
| D. | CCl4和I2都是非极性分子,而H2O是极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
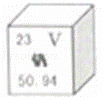
钒被誉为“合金中的维生素”,钒元素的部分信息如图.下列有关钒的说法正确的是( )
|
| A. | 属于非金属元素 | B. | 原子序数为23 |
|
| C. | 原子核外电子数为28 | D. | 相对原子质量为50.94g |
查看答案和解析>>
科目:高中化学 来源: 题型:
聚乙炔衍生物分子M的结构简式及M在稀硫酸作用下的水解反应如图所示.下列有关说法不正确的是()
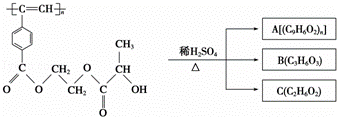
A. M与A均能使酸性高锰酸钾溶液和溴水褪色
B. B中含有羧基和羟基两种官能团,能发生消去反应和酯化反应
C. 1 mol M与热的烧碱溶液反应,可消耗2n mol NaOH
D. A、B、C各1 mol分别与金属钠反应,放出气体的物质的量之比为1:2:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com