
科目:高中化学 来源:2015-2016学年河南省高二下期末化学试卷(解析版) 题型:选择题
《本草纲目拾遗》中在药物名“鼻冲水”条目下写到:贮以玻璃瓶,紧塞其口,勿使泄气,则药力不减。气甚辛烈,触人脑,非有病不可嗅;在“刀创水”条目下写到:治金创,以此水涂伤口,即敛合如故。这里所说的“鼻冲水”、“刀创水”分别指的是( )
A.氢氟酸、食盐水 B.氨水、碘酒
C.石灰水、硝酸 D.稀硫酸、食醋
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期末化学试卷(解析版) 题型:选择题
已知25 ℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,该条件下向100 mL的CaSO4饱和溶液中,加入400 mL 0.01 mol·L -1 的Na2SO4溶液,针对此过程的下列叙述正确的是(忽略混合过程中的体积变化)

A.溶液中析出CaSO4沉淀,最终溶液中c(SO42-)较原来大
B.溶液中无沉淀析出,溶液中c(Ca2+ )、c(SO42-)都变小
C.溶液中析出CaSO4沉淀,溶液中c(Ca2+ )、c(SO 42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO 42-)较原来大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二下期末化学试卷(解析版) 题型:选择题
为了证明液溴与苯发生的反应是取代反应,有如图所示装置。则装置A中盛有的物质是 ( )
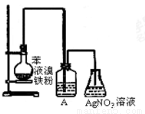
A.水 B.CCl4 C.NaOH D.NaI溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二下期末化学试卷(解析版) 题型:选择题
既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中混有的乙烯的方法是 ( )
A.在导管口处点燃
B.通入足量高锰酸钾溶液中
C.通入足量溴水中
D.在一定条件下与H2反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二下期末化学试卷(解析版) 题型:填空题
一般较强酸可制取较弱酸,这是复分解反应的规律之一。
已知在常温下:K(C6H5OH)=1.2×10-10 K(CH3COOH)=1.8×10-5
K(H2CO3)=4.3×10-7 K(HCO3-)=5.6×10-11 K(HCN)=4.9×10-10
(1)请根据上述信息求Na2CO3+C6H5OH NaHCO3+C6H5ONa的化学平衡常数K=_________;
NaHCO3+C6H5ONa的化学平衡常数K=_________;
(2)常温下某电解质溶解在水中后,溶液中的c(H+)=10-9mol•L-1,则该电解质可能是____(填序号);
A. CuSO4
B. HCl
C. Na2S
D.NaOH
E.K2SO4
(3)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性
①浓度为1.0×l0-3mol.L-1的氨水bL;
②c(OH-)=1.0×10-3mol.L-l的氨水cL;
③c(OH-)=1.0×10-3mol•L-1的氢氧化钡溶液dL.
则a、b、c、d之间由大到小的关系是:_________;
(4)一定温度下,向等体积纯水中分别加入等物质的量的CH3COONa和NaCN,两溶液中阴离子的总物质的量分别为n1和n2,则n1和n2的关系为n1_______n2(填“>”、“<”或“=”);
(5)己知常温时Ksp(AgCl)=1.8×10-10mol2•L-2,向50mL 0.018mol•L-1的AgNO3溶液中加入相同体积0.020mol•L-1的盐酸,则c(Ag+)=_______,此时所得混合溶液的pH=_________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二下期末化学试卷(解析版) 题型:选择题
己烯雌酚是人工合成的非甾体雌激素物质,主要用于治疗雌激素低下症及激素平衡失调所引起的功能性出血等,如图所示分别取1mol己烯雌酚进行4个实验。下列对实验数据的预测与实际情况吻合的是

A.①中生成7 mol H2O
B.②中无CO2生成
C.③中最多消耗3 mol Br2
D.④中发生消去反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期末化学试卷(解析版) 题型:填空题
(1)常温下,如果取0.1mol•L-1HA溶液与0.1mol•L-1NaOH溶液等体积混合(混合后溶液体积的变化忽略不计),测得混合液的pH=8。
①混合液中由水电离出的OH-浓度与0.1mol•L-1NaOH溶液中由水电离出的OH-浓度之比为_________;
②已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH _____7(填“<”、“>”或“=”);相同温度下,等物质的量浓度的下列四种盐溶液按pH由大到小的排 列顺序为_________(填序号)。
a.NH4HCO3 b.NH4A c.(NH4)2CO3 d.NH4Cl.
(2)清洁能源具有广阔的开发和应用前景,可减小污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池。
一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)?CH3OH(g)△H=-105kJ•mol-1.向体积为2L的密闭容器中充入2molCO和4molH2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:

①Ⅱ和Ⅰ相比,改变的反应条件是_________;
②反应Ⅰ在6min时达到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)=_________;
③反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=_________;
④比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1_____T3(填“>”“<”“=”),判断的理由是_________;
(3)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。图甲所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-(O2+4e=2O2-)

①c电极为_________正极,d电极上的电极反应式为_________;
②图乙是用惰性电极电解100mL 0.5mol•L-1 CuSO4溶液,a电极上的电极反应式为_________;若a电极产生56mL(标准状况)气体,则所得溶液的pH=_________(不考虑溶液体积变化),若要使电解质溶液 恢复到电解前的状态,可加入_________(选填字母序号)
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津一中高二下期末化学试卷(解析版) 题型:实验题
已知:以铜作催化剂,用空气氧化醇制取醛,事实上是空气先与铜反应生成氧化铜,热的氧化铜再氧化醇生成醛。某实验室中用甲醇、水、空气和铜粉(或氧化铜)制取甲醛溶液。左表给出甲醇、甲醛的沸点和水溶性:
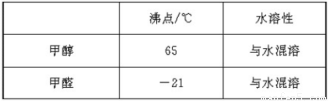
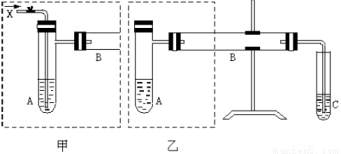
上图是两个同学设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如甲和乙所示,请回答下列问题:
(1)在仪器组装完成后,加装试剂前必须要进行的操作是____________________。
(2)若按甲装置进行实验,则通入 A 的 X 是__________,B 中发生反应的化学方程式为_____________。
(3)若按乙装置进行实验,则 B 管中应装入的物质是__________,B 中发生反应的化学方程式为___________。
(4)试管 C中应装入的试剂是__________。
(5)两套装置中都需要加热的仪器有__________(填 A、B、C)。
(6)若欲得到较浓的甲醛溶液,你认为选用哪套装置较好?__________(填“甲”或“乙”)。
(7)请设计简单的实验,检验实验后 C 中所得液体确为甲醛溶液。简述所用试剂、操作、现象及结论。___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com