
【题目】由芳香烃X合成一种功能高分子H的过程如下。(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H的链节组成为C7H5NO。
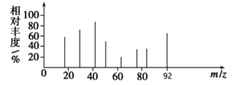
已知:I.芳香烃X用质谱仪测出的质谱图如图所示

诮根据所学知识与本题所给信息回答下列问题:
(1)阿司匹林中含氧官能团的名称为___________
(2)反应③和④的类型分别是_________、_________
(3)H的结构简式是_________
(4)反应⑤的化学方程式是_________
(5)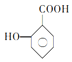 化学名称为______,它的一种同系物
化学名称为______,它的一种同系物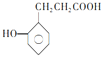 有多种同分异构体,其中符合下列要求的共有________种(不考虑立体异构),写出其中核磁共振氢谱为6组峰,且峰面积比为2:2:2:2:1:1的结构简式_______;
有多种同分异构体,其中符合下列要求的共有________种(不考虑立体异构),写出其中核磁共振氢谱为6组峰,且峰面积比为2:2:2:2:1:1的结构简式_______;
①能与NaHCO3反应放出CO2
②能与FeCl3溶液发生显色反应
③苯环上的一取代物有两种
(6)请用合成反应流程图表示出由A和其他无机物合成![]() 最合理的方案_____________。
最合理的方案_____________。
【答案】 酯基 羧基 还原反应 缩聚反应 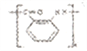
 邻羟基苯甲酸 16
邻羟基苯甲酸 16 ![]()
【解析】根据质谱仪测出的质谱图可知,芳香烃X的分子量为92,与氯气发生取代反应生成一氯代物A,所以X为甲苯。
(1)根据阿司匹林的结构简式可知,含氧官能团为酯基 羧基;正确答案:酯基 羧基。
(2) X为甲苯,发生硝化反应生成有机物F, 有机物F中的甲基被酸性高锰酸钾溶液溶液氧化为羧基,然后硝基在铁、盐酸作用下被还原为氨基,所以反应③为还原反应;芳香氨基酸发生缩聚反应生成高分子,反应④为缩聚反应;正确答案:还原反应;缩聚反应。
(3)林氨基苯甲酸在一定条件下发生缩聚反应生成高分子H,结构简式是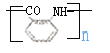 ;正确答案:
;正确答案: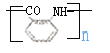 。
。
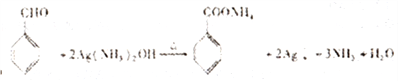
(4)有机物A为一氯甲苯,发生取代反应生成苯甲醇,在铜作催化剂条件下氧化为苯甲醛,苯甲醛被银氨溶液氧化,化学方程式是:![]() +2Ag(NH3)2OH→
+2Ag(NH3)2OH→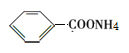 +2Ag+3NH3+H2O;正确答案:
+2Ag+3NH3+H2O;正确答案:![]() +2Ag(NH3)2OH→
+2Ag(NH3)2OH→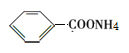 +2Ag+3NH3+H2O。
+2Ag+3NH3+H2O。
(5)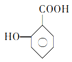 该有机物属于羧酸,羟基作为取代基, 化学名称为邻羟基苯甲酸;它的一种同系物
该有机物属于羧酸,羟基作为取代基, 化学名称为邻羟基苯甲酸;它的一种同系物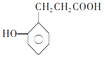 有多种同分异构体,①能与NaHCO3反应放出CO2,含有羧基;②能与FeCl3溶液发生显色反应,含有酚羟基;③苯环上的一取代物有两种,环上有2种氢;因此这样结构有:苯环上含有(1个-OH 和1个–CH2CH2COOH)结构有1种;苯环上有(1个-OH 和1个–CH(CH3)COOH)结构有1种;含有苯环,且环上有2个甲基在邻位,则-COOH 和 –OH的异构体有5种;含有苯环,且环上有2个甲基在间位,则-COOH 和 –OH的异构体有6种;含有苯环,且环上有2个甲基在对位,则-COOH 和–OH的异构体有3种;共计有16种;其中核磁共振氢谱为6组峰,且峰面积比为2:2:2:2:1:1的结构简式:
有多种同分异构体,①能与NaHCO3反应放出CO2,含有羧基;②能与FeCl3溶液发生显色反应,含有酚羟基;③苯环上的一取代物有两种,环上有2种氢;因此这样结构有:苯环上含有(1个-OH 和1个–CH2CH2COOH)结构有1种;苯环上有(1个-OH 和1个–CH(CH3)COOH)结构有1种;含有苯环,且环上有2个甲基在邻位,则-COOH 和 –OH的异构体有5种;含有苯环,且环上有2个甲基在间位,则-COOH 和 –OH的异构体有6种;含有苯环,且环上有2个甲基在对位,则-COOH 和–OH的异构体有3种;共计有16种;其中核磁共振氢谱为6组峰,且峰面积比为2:2:2:2:1:1的结构简式:![]() ;正确答案:邻羟基苯甲酸; 16;
;正确答案:邻羟基苯甲酸; 16;![]() 。
。
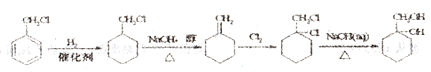
(6)有机物A为一氯甲苯,发生加成反应生成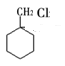 ,该有机物再发生消去反应生成
,该有机物再发生消去反应生成![]() ,
,![]() 与氯气发生加成生成
与氯气发生加成生成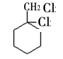 ,
, 再发生取代反应生成
再发生取代反应生成![]() ;合成流程如下:
;合成流程如下: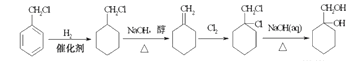 ;正确答案:
;正确答案:


科目:高中化学 来源: 题型:
【题目】某二元弱碱B(OH)2(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀B(OH)2溶液中滴加等浓度盐酸溶液,B(OH)2、B(OH)+、B2+的浓度分数δ随溶液POH[POH=-lgc(OH)-]变化的关系如图,以下说法正确的是
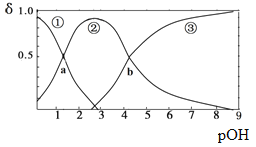
A. 交点a处对应加入的盐酸溶液的体积为5mL
B. 当加入的盐酸溶液的体积为10mL时存在c(Cl-)>c(B(OH)+)>c(H+)>c(OH-)>c(B2+)
C. 交点b处c(OH)=6.4×10-5
D. 当加入的盐酸溶液的体积为15mL时存在:c(Cl-)+c(OH-)= c(B2+)+c(B(OH)+)+ c(H+),
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氧(NOCl)是有机合成中的重要试剂,工业上可由NO与Cl2反应制得,回答下列问题:
(1)NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_______
(2)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰气,涉及如下反应:
2NO2(g)+NaCl(s)![]() NaNO3(s)+NOCl(g) ΔH1 K1;
NaNO3(s)+NOCl(g) ΔH1 K1;
4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) ΔH2 K2;
2NaNO3(s)+2NO(g)+Cl2(g) ΔH2 K2;
2NO(g)+Cl2(g)![]() 2NOCl(g) ΔH3 K3;
2NOCl(g) ΔH3 K3;
则ΔH3=_____(用ΔH1和ΔH2表示),K3=______(用K1和K2表示)
(3)25℃时,向2L带气压计的恒容密闭容器中通入0.08molNO和0.04molCl2发生反应:2NO(g)+Cl2(g)=2NOCl(g)ΔH
①测得其压强(p)随时间(t)的变化如图I曲线a所示(反应达到平衡时的温度与起始温度相同),则ΔH___0(填“>”或“<”);若其他条件相同,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图I曲线b所示,则改变的条件是______。
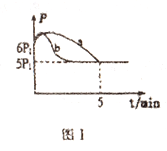
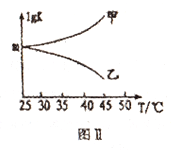
②图Ⅱ是甲、乙同学描绘上述反应平衡常数的对数值(lgK)与温度的变化关系,其中正确的曲线是______ (填“甲”或“乙”);m值为_______
(4)NO可用间接电化学法除去,其原理如图3所示
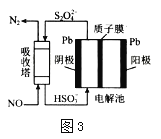
①阴极的电极反应式为_________
②吸收塔内发生反应的离子方程式为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属A及其化合物之间有如下的转化关系:
(1)写出A、B的化学式:A_______,B_________。
(2)写出B→D的化学方程式_______________________________。
(3)写出B→C的离子方程式________________________________。
(4)写出E→C的化学方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝、铁是常见的两种金属,它们的单质及化合物在生活生产中处处可见。
(1)过量的铁和稀硝酸发生反应,产物是Fe(NO3)2和NO,写出该反应的化学方程式_________________________________________________。
(2)实验室配制FeSO4溶液时,如果没有隔绝空气,FeSO4会被氧化为___________(填化学式)。在该溶液中加入___________试剂,看到_____________________现象,证明溶液变质。
(3)已知:Ba(AlO2)2可溶于水,下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。

由图可知c点的沉淀是___________(填化学式),已知a-b时存在的沉淀是Al(OH)3和BaSO4,a点时,n(BaSO4)_____ n(Al(OH)3)(填“>”“<”“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含有少量NaCl、Na2SO4、Na2CO3、泥沙(SiO2)等杂质的NaNO3固体,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。
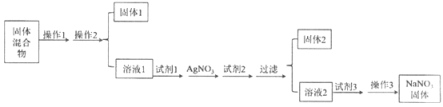
(1)操作1、操作3的名称分别是_________、_________。
(2)试剂1和试剂2分别是_________、_________。固体2中除了含有AgCl,还有_________(答全)。
(3)试剂3加入后发生的离子反应方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种重要的化工原料,可用于合成可降解的高聚物PES树脂以及具有抗肿瘤活性的化合物K。
是一种重要的化工原料,可用于合成可降解的高聚物PES树脂以及具有抗肿瘤活性的化合物K。

已知:i.R1CO18OR2+R3OH![]() R1COOR3+R218OH
R1COOR3+R218OH
ii. 
ⅲ.  (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)
(1)A的名称是_________;C的官能团的名称是_________。
(2)B分子为环状结构,核磁共振氢谱只有一组峰,B的结构简式为_________ .
(3)E分子中含有两个酯基,且为顺式结构,E的结构简式为_________ .
(4)反应①的化学方程式为_________ 。
(5)试剂a的结构简式为_________;反应②所属的反应类型为________反应。
(6)已知:  。以1,3-丁二烯为起始原料,结合已知信息选用必要的无机试剂合成
。以1,3-丁二烯为起始原料,结合已知信息选用必要的无机试剂合成![]() 。将以下合成路线补充完整:_________________
。将以下合成路线补充完整:_________________

(7)已知氨基(-NH2)与羟基类似,也能发生反应i。在由J制备K的过程中,常会产生副产物L。L分子式为C16H13NO3,含三个六元环,则L的结构简式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com