
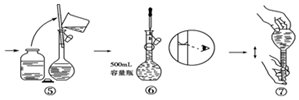
| A. | ⑤⑥ | B. | ⑦ | C. | ⑥ | D. | ⑤⑥⑦ |
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 电池工作时,锌失去电子 | |
| B. | 电池工作时,电子由正极通过外电路流向负极 | |
| C. | 电池正极的电极反应式为2MnO2(s)+H2O(l)+2e-═Mn2O3(s)+2OH-(aq) | |
| D. | 外电路中每通过0.1 mol电子,锌的质量理论上减少6.5 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 萃取碘水中碘,用无毒无害的酒精代替四氯化碳更加环保 | |
| C. | 不可以用过滤的方法除去粗盐中的CaCl2、MgCl2等杂质 | |
| D. | 用丁达尔效应区分FeCl3溶液和Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Al2(SO4)3═3Al3++2SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | NaHSO4═Na++H++SO42- | D. | K2MnO4═2K++MnO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中c(SO42-)=0.2mol/L | |
| B. | 该溶液中c(SO42-)=2c(Al3+) | |
| C. | 该溶液中:3c(Al3+)+c(K+)+c(H+)=2c(SO42-) | |
| D. | 向该溶液中加入2L0.1mol/LBa(OH)2溶液,生成的沉淀为BaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H2 | B. | C4H6 | C. | C3H4 | D. | C4H8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com