
 CO(g)+H2(g) △H=+131.3KJ.mol-1[各容器中C(s)均足量],在某时刻测得有关物质的浓度及正、逆反应速率的关系如下表。下列说法不正确的是
CO(g)+H2(g) △H=+131.3KJ.mol-1[各容器中C(s)均足量],在某时刻测得有关物质的浓度及正、逆反应速率的关系如下表。下列说法不正确的是 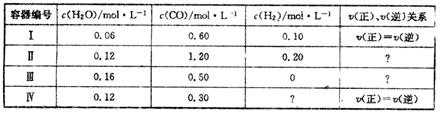
| A.在容器Ⅱ中,v(正)<v(逆) |
| B.在容器Ⅳ中,H2的浓度为0.40 mol.L-1 |
| C.在容器Ⅲ中, 反应达到平衡时吸收的热量为13.13 KJ |
| D.若将平衡时容器Ⅰ、Ⅳ中的物质混合于容积为1L的容器中,则反应仍处于平衡状态 |
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源:不详 题型:单选题

 2 Z(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )
2 Z(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )| A.平衡时气体的平均摩尔质量:M(Ⅰ) <M(Ⅱ) |
| B.平衡时气体的密度:ρ(Ⅰ)>ρ(Ⅱ) |
| C.平衡时Ⅰ和Ⅱ中Z的百分含量z%(Ⅰ) > z% (Ⅱ) |
| D.平衡时气体的压强P(Ⅰ)<P (Ⅱ) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
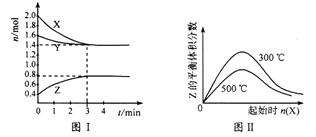
A.该反应的化学方程式为: 2X(g) + Y(g) 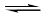 2Z(g) 2Z(g) |
| B.反应进行的前3min内,用X表示的平均反应速率v(x)=0.067mol/(L·min) |
| C.由图II可知,其他条件不变,增大X的量时Y的转化率先增大后减小 |
| D.其他条件不变,升髙温度,平衡逆向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g);△H<0。若起始时,M、N容积相同。下列说法正确的是( )
2C(g);△H<0。若起始时,M、N容积相同。下列说法正确的是( )
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
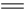 C(g) +D(g) △H-T△S="(-4500+11T)" J/mol,要防止反应发生,温度必须:
C(g) +D(g) △H-T△S="(-4500+11T)" J/mol,要防止反应发生,温度必须:| A.高于409K | B.低于136 K |
| C.高于136K而低于409K | D.低于409K |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于水的时间/s |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | t1 |
| E | 2 | 颗粒 | 15 | t2 |
| F | 2 | 粉末 | 15 | t3 |
| G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g)+ H2(g) ;△H<0。在850℃时,平衡常数K=1。
CO2(g)+ H2(g) ;△H<0。在850℃时,平衡常数K=1。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3。请填写下列空白:
2SO3。请填写下列空白: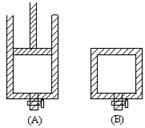
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2C(g) △H<0
2C(g) △H<0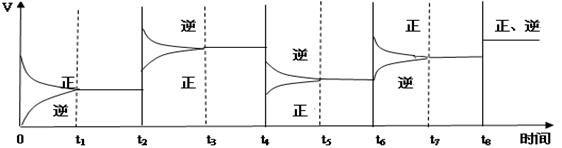
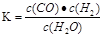
| A.容器中气体的平均相对分子质量不随时间而变化 |
| B.υ正(H2O)=υ逆(H2) |
| C.容器中气体的密度不随时间而变化 |
| D.容器中总的物质的量不随时间而变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com