
【题目】一定温度下,下列溶液的离子浓度关系式正确的是
A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5mol·L—1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
D. pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
【答案】D
【解析】
A.H2S溶液中分步电离,H2S![]() H++HS-,HS-
H++HS-,HS-![]() H++S2-,根据电荷守恒知c(H+)= c(HS-)+2 c(S2-)+ c(OH-)=1×10—5mol·L—1 ,A项错误;B.加水稀释促进一水合氨的电离,pH=a的氨水,稀释10倍后,其pH=b,则a<b+1,B项错误;C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合,溶液中存在电荷守恒,c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-),C项错误;D.酸性大小为CH3COOH>H2CO3>HClO,组成盐的酸根对应的酸越弱,该盐的水解程度越大,相同浓度时溶液的碱性越强。pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液,盐的浓度:①>②>③,c(Na+):①>②>③,D项正确;故选D。
H++S2-,根据电荷守恒知c(H+)= c(HS-)+2 c(S2-)+ c(OH-)=1×10—5mol·L—1 ,A项错误;B.加水稀释促进一水合氨的电离,pH=a的氨水,稀释10倍后,其pH=b,则a<b+1,B项错误;C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合,溶液中存在电荷守恒,c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-),C项错误;D.酸性大小为CH3COOH>H2CO3>HClO,组成盐的酸根对应的酸越弱,该盐的水解程度越大,相同浓度时溶液的碱性越强。pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液,盐的浓度:①>②>③,c(Na+):①>②>③,D项正确;故选D。


 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E 分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
(1)实验室常用A的饱和溶液制备微粒直径为1nm~l00nm的红褐色液相分散系。则该反应的化学方程式为____________________________。
(2)B为地壳中含量最高的金属元素的氯化物,向50.0mL6mol/L的B溶液中逐滴滴入100mL某浓度的KOH溶液,若产生7.8g白色沉淀,则加入的KOH溶液的浓度可能为________________。
(3)将A、B中两种金属元素的单质用导线连接,插入一个盛有KOH溶液的烧杯中构成原电池,则电池反应为_______________________。
(4)C、D、E均是短周期中同一周期元素形成的单质或化合物,常温下D为固体单质,C和E均为气态化合物,且可发生反应:C+D![]() E。将一定量的气体C通入某浓度的KOH溶液得溶液F,向F溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(C)的关系如图所示,则生成F的离子方程式______________________。
E。将一定量的气体C通入某浓度的KOH溶液得溶液F,向F溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(C)的关系如图所示,则生成F的离子方程式______________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同位素的应用十分广泛,如14C的放射性可用于考古断代,15N可用于生物大分子的空间结构的测定。有关叙述正确的是
A.13C与15N有相同的中子数B.14N与14C互为同位素
C.13C与14C为同一种核素D.15N的核外电子数比中子数少1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
(1)该反应的化学方程式为_______________________________;
(2)反应开始至2min,以气体Z表示的平均反应速率为________________;
(3)混合气体的平均相对分子质量比起始时___________;(填“大”,“小”或“相等”)
平衡时容器内混合气体密度比起始时______(填“大”,“小”或“相等”)
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=___________.

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符合的是
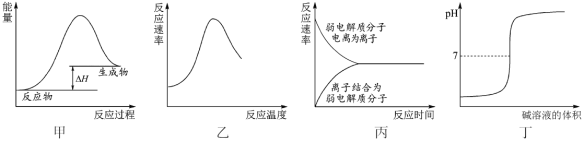
A.图甲表示燃料燃烧反应的能量变化
B.图乙表示酶催化反应的反应速率随反应温度的变化
C.图丙表示弱电解质在水中建立电离平衡的过程
D.图丁表示强碱滴定强酸的滴定曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酸可与水反应生成乳酸,化学方程式如下,下列说法正确的是

A. 该反应为加成反应,没有副产物生成
B. 可用Br2/CCl4溶液鉴别丙烯酸和乳酸
C. 丙烯酸与乳酸都属于有机酸,两者不发生反应
D. 1mol乳酸分别与足量Na、NaOH、NaHCO3反应,消耗三者物质的量之比为2:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示法正确的是( )
A. 等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B. 已知2C(s)+O2(g)=2CO(g);ΔH=-221.0 kJ/mol。则C(碳)的燃烧热为△H=—110.5 kJ/mol
C. 在稀溶液中: H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ
D. 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) ΔH=-285.8 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学不小心将KCl溶液中混入了KBr,为了除去杂质,得到KCl固体,该同学采用的试剂和采用的方法最合适的是( )
试剂:a.氯水 b.溴水 c.碘水 方法:①通入热空气 ②加入氯水振荡 ③过滤 ④蒸干
A.a ①
B.b ②
C.c ③
D.a ④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了如下装置用于制取SO2和验证SO2的性质。已知:1.0mol·L-1Fe(NO3)3溶液的pH=1。

(1)装置A中用于添加浓硫酸的仪器名称为___,导管①的作用是_______。
(2)B、C、D三个装置分别先后验证了SO2的哪些性质_____(填字母)。
A. 吸附性、酸性、还原性 B. 还原性、酸性、还原性
C. 漂白性、酸性、还原性 D. 漂白性、酸性、氧化性
(3)实验前鼓入N2的目的是________。
(4)装置E中产生了白色沉淀,其成分是____(填化学式),分析E中产生白色沉淀的可能原因(写两种)。可能①:_____。可能②:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com