
| A.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,再将不溶物用稀盐酸溶解去除 |
| B.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解 |
| C.向纯水中加入盐酸或降温都能使水的离子积减小,电离平衡逆向移动 |
| D.反应2A(g) + B(g) =" 3C" (s) + D(g)在一定条件下能自发进行,说明该反应的ΔH>0 |
科目:高中化学 来源:不详 题型:单选题
| A.催化剂通过降低化学反应的焓变加快化学反应速率 |
| B.铅蓄电池充电时.标有“一”的电极应与电源的负极相连 |
| C.温度保持不变.向水中加入钠盐对水的电离一定没有影响 |
| D.向醋酸钠溶液中加水稀释时.溶液中所有离子浓度都减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 N2O4(g) △H =-52.7kJ·mol-1
N2O4(g) △H =-52.7kJ·mol-1
 N2O4已经达到平衡。
N2O4已经达到平衡。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下能够进行的化学反应都是放热反应,高温下进行的反应都是吸热反应 |
| B.常温常压下,pH = 1的盐酸中约含有6.02×1023个氢离子 |
| C.常温常压下,0.5mol氮气和氢气的混合气体体积大于11.2L |
| D.原电池装置的正、负极可以是同一种金属 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
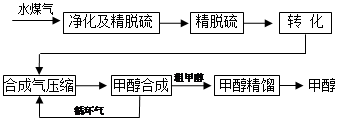
 CO(g)+H2(g),此反应是吸热反应。①此反应的化学平衡常数表达式为 ;
CO(g)+H2(g),此反应是吸热反应。①此反应的化学平衡常数表达式为 ;| A.加入C(s) | B.加入H2O(g) | C.升高温度 | D.增大压强 |
 CO (g)+2H2O (g) +519KJ。工业上要选择合适的催化剂,分别对X、Y、Z三种催化剂进行如下实验(其他条件相同)
CO (g)+2H2O (g) +519KJ。工业上要选择合适的催化剂,分别对X、Y、Z三种催化剂进行如下实验(其他条件相同) CH3OH(g)+181.6kJ。T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
CH3OH(g)+181.6kJ。T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:| 物质 | H2 | CO | CH3OH |
| 浓度/(mol·L-1) | 0.2 | 0.1 | 0.4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 |
| N2浓度/mol·L-1 | 4.00 | 3.70 | 3.50 | 3.36 | 3.26 | 3.18 | 3.10 | 3.00 | 3.00 | 3.00 |
| CO浓度/mol·L-1 | 0.00 | 0.90 | 1.50 | 1.92 | 2.22 | 2.46 | 2.70 | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=7的溶液一定是中性溶液 |
| B.能自发进行的化学反应,不一定是△H<0、△S>0 |
| C.吸热反应发生过程中要不断从外界获得能量,放热反应一定不需要吸收外界能量 |
| D.Ksp不仅与难溶电解质的性质和温度有关,而且与溶液中的离子浓度有关 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在船舶的外壳装上铜块可防止其发生电化学腐蚀 |
| B.MnO2、FeCl3和CuSO4都可加快H2O2的分解速率 |
| C.FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
| D.用惰性电极分别电解CuCl2溶液和MgCl2溶液分别得到单质Cu和Mg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com