
| A. | 乙烯与苯都能使溴水褪色,但褪色原理不同 | |
| B. | 1 mol乙烯与Cl2完全加成,然后与Cl2发生取代反应,共消耗氯气5mol | |
| C. | 溴水遇到乙醛溶液出现褪色现象,是因为它们发生了氧化反应 | |
| D. | 二氯甲烷存在两种不同的结构 |
分析 A.乙烯与溴发生加成反应,使溴水中水层褪色;苯萃取溴水的溴,使溴水中水层褪色;
B.1mol乙烯与Cl2完全加成,消耗氯气1mol,生成1mol1,2-二氯乙烷,1mol1,2-二氯乙烷与4molCl2发生取代反应,生成1mol六氯乙烷;
C.溴水具有氧化性,醛基具有还原性;
D.二氯甲烷为四面体结构,不存在同分异构体.
解答 解:A.乙烯与溴发生加成反应,使溴水中水层褪色,溴在苯的溶解度远远大于水中的溶解度,苯萃取溴水的溴,使溴水中水层褪色,二者褪色原理不同,故A正确;
B.1mol乙烯与Cl2完全加成,消耗氯气1mol,生成1mol1,2-二氯乙烷,1mol1,2-二氯乙烷与4molCl2发生取代反应,生成1mol六氯乙烷,故共消耗氯气5mol,故B正确;
C.溴水具有氧化性,醛基具有还原性,溴水能与乙醛发生氧化还原反应,使溴水褪色,故C正确;
D.因甲烷是正四面体结构,故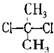 与
与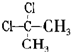 不存在同分异构体,为同一物质,故D错误,
不存在同分异构体,为同一物质,故D错误,
故选D.
点评 本题考查有机物的结构与性质、有机物的鉴别等,为高频考点,把握常见有机物的官能团及性质为解答的关键,注重基础知识的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:8 | B. | 8:1 | C. | 2:5 | D. | 5:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液是电中性的,胶体是带电的 | |
| B. | 两者的分散质微粒均能透过半透膜和滤纸 | |
| C. | 溶液中溶质分子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 | |
| D. | 一束光线分别通过溶液和胶体时,后者会出现明显的“光亮的通路”,前者则没有 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
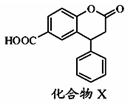
| A. | 分子中两个苯环一定处于同一平面 | |
| B. | 不能与饱和Na2CO3溶液反应 | |
| C. | 在酸性条件下水解,水解产物只有一种 | |
| D. | 1mol化合物X最多能与7molH2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl晶体、BaSO4 | B. | 铜、二氧化硫 | C. | 硫酸溶液、HCl | D. | 熔融的KNO3、酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
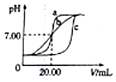 某班学生用0.1mol•L-1盐酸和0.1mol•L-1NaOH溶液反应测定酸碱滴定曲线,甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示,下列说法错误的是( )
某班学生用0.1mol•L-1盐酸和0.1mol•L-1NaOH溶液反应测定酸碱滴定曲线,甲、乙、丙三组同学锥形瓶中的溶液所取体积均为20.00mL,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示,下列说法错误的是( )| A. | 乙组同学操作上的不足是在滴定终点附近测试和记录pH的间隔太大 | |
| B. | 甲组同学滴定时选用的滴定管为酸式滴定管 | |
| C. | 乙和丙两组同学的操作均存在不足或失误 | |
| D. | 丙组同学可能是用待测液润洗了锥形瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
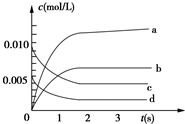 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com