
 ��Ǧ���ص��ס��ҵ����е���Һ����֪Ǧ���ص��ܷ�ӦΪ��Pb+PbO2+2H2SO4�T2PbSO4+2H2O�����һ��ʱ�����c����d�������ֱ�μӷ�̪�Լ���c��������Һ��죬����˵����ȷ���ǣ�������
��Ǧ���ص��ס��ҵ����е���Һ����֪Ǧ���ص��ܷ�ӦΪ��Pb+PbO2+2H2SO4�T2PbSO4+2H2O�����һ��ʱ�����c����d�������ֱ�μӷ�̪�Լ���c��������Һ��죬����˵����ȷ���ǣ�������| A�� | d��Ϊ���� | |
| B�� | �ŵ�ʱǦ���ظ����ĵ缫��ӦʽΪ��PbO2+4H++SO42-+4e-�TPbSO4+2H2O | |
| C�� | �����ü׳ؾ���ͭ��b��ӦΪ��ͭ | |
| D�� | ���缫���Ͼ�Ϊʯī��������6.4g Cuʱ�����ع���������3.36L����״���£� |
���� A�����һ��ʱ�����c����d�������ֱ�μӷ�̪�Լ���c��������Һ��죬˵��C�������м����ɣ����õ缫�������ӷŵ磬�õ缫����������d����������a������b��������
B���ŵ�ʱ��������ʧȥ���ӷ���������Ӧ��
C����⾫��ͭʱ����ͭ����������ͭ��������
D������ת�Ƶ��Ӻ���������֮��Ĺ�ϵʽ���㣮
��� �⣺A�����һ��ʱ�����c����d�������ֱ�μӷ�̪�Լ���c��������Һ��죬˵��C�������м����ɣ����õ缫�������ӷŵ磬�õ缫����������d������������A����
B���ŵ�ʱ��Ǧ���ظ����ĵ缫��ӦʽΪ��Pb��s��+SO42-��aq��-2e-=PbSO4 ��s������B����
C�����һ��ʱ�����c����d�������ֱ�μӷ�̪�Լ���c��������Һ��죬˵��C�������м����ɣ����õ缫�������ӷŵ磬�õ缫����������d����������a������b����������⾫��ͭʱ����ͭ����������ͭ������������b��ӦΪ��ͭ����C��ȷ��
D�����ĸ��缫���Ͼ�Ϊʯī����������������������������������ͭ���ҵ�������������������������������������������6.4 g Cuʱ��ת�Ƶ�����0.2mol����������0.1mol������0.1mol������0.05mol���������������й���������5.6 L����״���£�������D����
��ѡC��
���� ���⿼���˵��ԭ�����ѶȲ�����ȷ�жϵ��ص��������ǽⱾ��Ĺؼ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | ʵ������ | ʵ��Ŀ�� |
| A | ��ƽ�й����� | ���������Һ���Ȼ�����Һ |
| B | ����CaCO3��ĩ����ַ�Ӧ����� | ��ȥCaCl2��Һ�е�FeCl3 |
| C | ͨ�����յ�Cu��ĩ���ռ����� | ��ȥN2�е�����O2 |
| D | ����ϡ���ᣬͬʱ��pH�Ʋⶨ����Һ������ | ��ȥKNO3��Һ�е�KOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | ������ | C�� | ʳ�� | D�� | ʯ��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
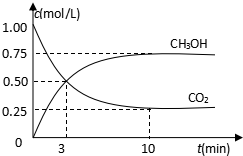 �������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ�Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬��485��ʱ�������Ϊ1L���ܱ������У�����1ol CO2��3mol H2��һ�������·�����Ӧ�ϳɼ״���
�������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ�Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬��485��ʱ�������Ϊ1L���ܱ������У�����1ol CO2��3mol H2��һ�������·�����Ӧ�ϳɼ״����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCl | B�� | NaOH | C�� | AgNO3 | D�� | BaCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ڵ��ھƾ��е��ܽ�ȴ����Կ��þƾ��ѵ�ˮ�еĵ���ȡ���� | |
| B�� | �������ʱ��Ӧʹ�¶ȼ�ˮ����������ƿ��֧�ܿڴ� | |
| C�� | ʹ������ƿǰ������Ƿ�©ˮ | |
| D�� | ��������ʱ������ʹ������е�ˮ����ȫ���ɺ��ֹͣ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
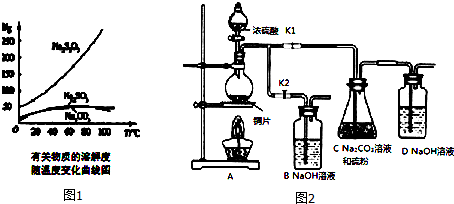
| ��� | 1 | 2 | 3 | 4 |
| ��Һ�����/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| ����I2����Һ�����/mL | 19.99 | 19.98 | 17.13 | 20.03 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
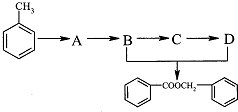
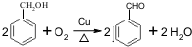
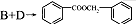 �Ļ�ѧ����ʽΪ
�Ļ�ѧ����ʽΪ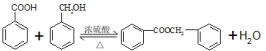
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ۢ� | B�� | �ڢݢ� | C�� | �ۢ� | D�� | �ۢܢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com