
【题目】元素X的原子有3个电子层,最外层有4个电子。这种元素位于周期表的
A. 第4周期ⅢA族 B. 第4周期ⅦA族
C. 第3周期ⅣB族 D. 第3周期ⅣA族
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式,书写正确的是
A.用惰性电极电解熔融氯化钠:2Cl-+ 2H2O![]() Cl2↑+ H2↑+ 2OH-
Cl2↑+ H2↑+ 2OH-
B.铁粉溶于稀硫酸:2Fe + 6H+ = 2Fe3+ + 3H2↑
C.用 CuSO4 溶液吸收 H2S:Cu2+ + H2S = CuS↓+ 2H+
D.向 NH4HSO4 溶液中滴加少量的 Ba(OH)2 溶液:NH4++H++SO42-+Ba2++2OH-=BaSO4↓+NH3H2O+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置合理且能达到实验目的的是

A. 实验室用装置①制取氨气
B. 装置②将化学能转化为电能
C. 装置③可用于分离沸点相差较大的互溶液体混合物
D. 装置④可用于Fe(OH)2的制取,并能防止Fe(OH)2被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列热化学方程式:
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ/mol
②H2(g)+![]() O2(g)===H2O(l) ΔH2=-285.8 kJ/mol
O2(g)===H2O(l) ΔH2=-285.8 kJ/mol
③CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH3=-870.3 kJ/mol
可以计算出2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为( )
A.ΔH=+244.1 kJ/mol B.ΔH=-488.3 kJ/mol
C.ΔH=-996.6 kJ/mol D.ΔH=+996.6 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分) 研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)对于反应:2SO2(g)+O2(g)![]() 2SO3(g);如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= ;υ(SO3)= 。
2SO3(g);如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= ;υ(SO3)= 。
(2)已知:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) ![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) ![]() SO3(g)+NO(g)的ΔH=______ kJ·mol-1。
SO3(g)+NO(g)的ΔH=______ kJ·mol-1。
(3)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是______。
a、体系压强保持不变 b、混合气体颜色保持不变
c、SO3和NO的体积比保持不变 d、每消耗1 mol SO3的同时生成1 mol NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是
A.10mL质量分数为98%的H2SO4,用10mL水稀释后,H2SO4的质量分数大于49%
B.地球上99%的溴蕴藏在大海中,故溴被称为“海洋元素”
C.在标况下,将22.4L氨气溶于1L水中,得到1mol/L的氨水
D.向两等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图1所示的关系,完成下列空白:
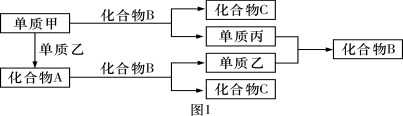
(1)向酚酞试液中加入化合物A的粉末,现象为 。
(2) 单质甲与化合物B反应的离子方程式为 。5.05 g单质甲—钾合金溶于200 mL水生成0.075 mol氢气,确定该合金的化学式为__ __。
(3)向20 mL某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1 mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图2图示两种情况。
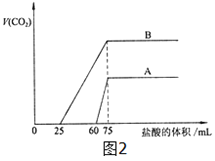
①由A确定滴加前60 mL的盐酸时,发生反应的离子方程式为 。
②由B表明,原溶液通入CO2气体后,所得溶液中的溶质的化学式为__ __。
③由A、B可知,两次实验通入的CO2的体积比为__ __。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中含有大量的H+和SO42-,则此溶液还能大量存在的离子组是
A.Na+、Fe2+、NO3-
B.Na+、Mg2+、NO3-
C.Cr2O72-、Ba2+、Cl-
D.K+、Na+、S2O32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一块镁铝合金投入到1 mol ·L-1 HC1溶液里,待合金完全溶解后,再往溶液里加入 1 mol L-1 NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如右图所示。下列说法中错误的是( )
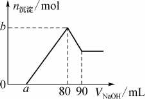
A.HC1溶液的体积为80 mL B.a的取值范围为0≤a<50
C.当a值为30时,b值为0.01 D.当a值为10时,b值为0.03
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com