
 ij�¶�ʱ����һ���ݻ�Ϊ2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ��
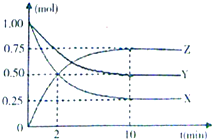
ij�¶�ʱ����һ���ݻ�Ϊ2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ ��1������ͼ֪�����ŷ�Ӧ�Ľ��У�X��Y�����ʵ������ٶ�Z�����ʵ�����������X��Y�Ƿ�Ӧ�Z�������10minʱ��Ӧ�ﵽƽ��״̬����μӷ�Ӧ�ġ�n��X��=��1.00-0.25��mol=0.75mol����n��Y��=��1.00-0.50��mol=0.50mol����n��Z��=��0.75-0��mol=0.75mol��ͬһ���淴Ӧ��ͬһʱ����ڲμӷ�Ӧ�ĸ����ʵ����ʵ���֮�ȵ����������֮�ȣ�
��2��0-2min��Z��ƽ����Ӧ����=$\frac{\frac{��n}{V}}{��t}$��
��3�����º��������£������ѹǿ֮�ȵ��������ʵ���֮�ȣ���Ӧǰ����������ʵ���=1.00mol��2=2.00mol��ƽ�������������ʵ���=��0.25+0.50+0.75��mol=1.5mol��
��4��A����ͬ�����У�X��Y��Z��Ũ��֮�ȵ��������ʵ���֮�ȣ�
B���÷�Ӧ��X��Y�ļ�����֮��Ϊ3��2����X������������Y����������֮��Ϊ3��2ʱ�÷�Ӧ�ﵽƽ��״̬��
C����Z��Ũ�ȱ��ֲ���ʱ�����淴Ӧ������ȣ�
D�������¶����´ﵽƽ�⣬Z��Ũ�ȼ�С��ƽ�������ƶ��������¶�ƽ�������ȷ����ƶ���
��� ��1������ͼ֪�����ŷ�Ӧ�Ľ��У�X��Y�����ʵ������ٶ�Z�����ʵ�����������X��Y�Ƿ�Ӧ�Z�������10minʱ��Ӧ�ﵽƽ��״̬����μӷ�Ӧ�ġ�n��X��=��1.00-0.25��mol=0.75mol����n��Y��=��1.00-0.50��mol=0.50mol����n��Z��=��0.75-0��mol=0.75mol��ͬһ���淴Ӧ��ͬһʱ����ڲμӷ�Ӧ�ĸ����ʵ����ʵ���֮�ȵ����������֮�ȣ�����X��Y��Z�ļ�����֮��=0.75mol��0.50mol��0.75mol=3��2��3�����Ը÷�Ӧ����ʽΪ3X+2Y?3Z��
�ʴ�Ϊ��3X+2Y?3Z��
��2��0-2min��Z��ƽ����Ӧ����=$\frac{\frac{��n}{V}}{��t}$=$\frac{\frac{0.50mol-0}{2L}}{2min}$=0.125mol/��L��min�����ʴ�Ϊ��0.125mol/��L��min����
��3�����º��������£������ѹǿ֮�ȵ��������ʵ���֮�ȣ���Ӧǰ����������ʵ���=1.00mol��2=2.00mol��ƽ�������������ʵ���=��0.25+0.50+0.75��mol=1.50mol�����Է�Ӧ��ʼʱ��ƽ����ѹǿ֮��=2.00mol��1.50mol=4��3���ʴ�Ϊ��4��3��
��4��A����ͬ�����У�X��Y��Z��Ũ��֮�ȵ��������ʵ���֮��=0.25mol��0.50mol=0.75mol=1��2��3����A��ȷ��
B���÷�Ӧ��X��Y�ļ�����֮��Ϊ3��2����X������������Y����������֮��Ϊ3��2ʱ�÷�Ӧ�ﵽƽ��״̬�����Ե�X���������ʺ�Y�������������ʱ�÷�Ӧû�дﵽƽ��״̬����B����
C����Z��Ũ�ȱ��ֲ���ʱ�����淴Ӧ������ȣ����淴Ӧ�ﵽƽ��״̬����C��ȷ��
D�������¶����´ﵽƽ�⣬Z��Ũ�ȼ�С��ƽ�������ƶ��������¶�ƽ�������ȷ����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ����D����
��ѡBD��
���� ���⿼�黯ѧƽ����㼰��ѧƽ��״̬�жϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������������������ղμӷ�Ӧ�����ʵ���Ũ�ȱ仯��֮���������֮�ȵĹ�ϵ�ǽⱾ��ؼ���ע�⣺ֻ�з�Ӧǰ��ı��������������Ϊƽ��״̬�ж����ݣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Mg��OH��2 | B�� | Al��OH��3 | C�� | NaHCO3 | D�� | MgCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | �����еĺ��� ������ٷֱȣ� | ����ЧӦ ָ�� |
| CO2 | 0.03 | 1 |
| H2O | 1 | 0.1 |
| CH4 | 2��10-4 | 30 |
| N2O4 | 3��10-5 | 160 |
| O3 | 4��10-6 | 2000 |
| CCl2F2 | 4.8��10-8 | 25000 |
 �������̼ԭ�ӵĹ���ӻ�������sp�ӻ���1mol Fe ��CO��5�����к��ЦҼ�����ĿΪ10NA��
�������̼ԭ�ӵĹ���ӻ�������sp�ӻ���1mol Fe ��CO��5�����к��ЦҼ�����ĿΪ10NA���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ������������C9H10O2����ˮ����ζ������������ˮ�㾫�����쾫�ͣ���������ʳƷ��ҵ�У����Ʊ��������£�
������������C9H10O2����ˮ����ζ������������ˮ�㾫�����쾫�ͣ���������ʳƷ��ҵ�У����Ʊ��������£�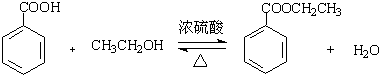 ��
��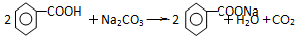 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
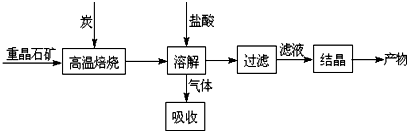
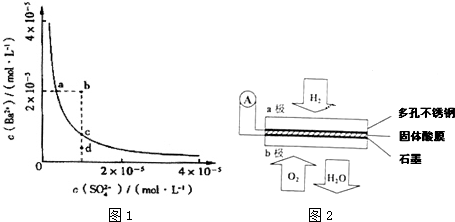
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com