
【题目】碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( ) 
A.洗气瓶中产生的沉淀是碳酸钡
B.从Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是亚硫酸钡
D.在Z导管口有红棕色气体出现
【答案】D
【解析】解:X为SO2和CO2 , Y为NO2 , XY混合之后SO2和NO2会发生氧化还原反应:SO2+NO2+H2O=H2SO4+NO
A、因H2SO4能与氯化钡反应生成BaSO4 , CO2与氯化钡不反应,没有BaCO3生成,故A错误;
B、因CO2不与氯化钡反应,从导管中逸出,故C错误;
C、因H2SO4能与氯化钡反应生成BaSO4 , 故C错误;
D、反应生成的NO在Z导管口与空气中的氧气反应生成NO2 , 呈红棕色,故D正确;
故选D.
据反应,判断X为SO2和CO2 , Y为NO2 , 生成NO2和SO2发生反应生成硫酸和NO,故有硫酸钡生成,由于硝酸的存在,二氧化碳与氯化钡不能生成碳酸钡沉淀从溶液中逸出.


科目:高中化学 来源: 题型:
【题目】2010年,中国首次应用六炔基苯在铜片表面合成了石墨炔薄膜(其合成示意图如图所示),其特殊的电子结构将有望广泛应用于电子材料领域.下列说法不正确的是( ) 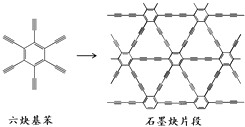
A.六炔基苯的化学式为C18H6
B.六炔基苯和石墨炔都具有平面型结构
C.六炔基苯和石墨炔都可发生加成反应
D.六炔基苯合成石墨炔属于加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4H2O).CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4H2O+NaCl
实验一:制备NaClO溶液
(1)将氯气通入到盛有NaOH的锥形瓶中,锥形瓶中发生反应的离子方程式是
;
实验二:制取水合肼(实验装置如图所示)控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充 分反应.加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分.(已知:N2H4H2O+2NaClO=N2↑+3H2O+2NaCl)
(2)分液漏斗中的溶液是(填标号A或B);
A.NaOH和NaClO混合溶液
B.CO (NH2) 2溶液
选择的理由是
实验三:测定馏分中肼含量
水合肼具有还原性,可以生成氮气.测定水合肼的质量分数可采用下列步骤:
a.称取馏分5.000g,加入适量NaHCO3固体,经稀释、转移、定容等步骤,配制250mL溶液.
b.移取25.00mL于锥形瓶中,加入10mL水,摇匀.
c.用0.2000mol/L碘溶液滴定至溶液出现微黄色且半分钟内不消失,滴定过程中,溶液的pH保持在6.5左右.记录消耗碘的标准液的体积.
d.进一步操作与数据处理
(3)水合肼与碘溶液反应的化学方程式;滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是
(4)滴定时,碘的标准溶液盛放在 滴定管中(选填:“酸式”或“碱式”);若本次滴定消耗碘的标准溶液为18.00mL,馏分中水合肼(N2H4H2O)的质量分数为(保留三位有效数字);
(5)为获得更可靠的滴定结果,步骤d中进一步操作主要是: . 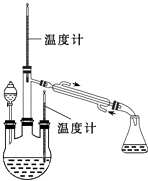
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】6﹣羰基庚酸是一种重要的化工中间体,其合成路线如下: 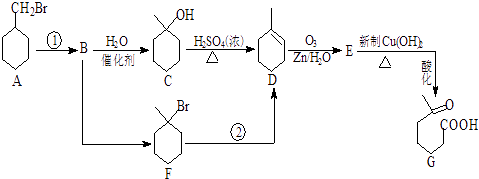
已知: 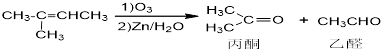
(1)C→D的反应类型是 .
(2)下列说法中正确的是 . (填字母)
a.C能被催化氧化成酮
b.D不能使酸性高锰酸钾溶液褪色
c.Ni催化下1mol E最多可与2molH2加成
d.G既能发生取代反应,又能发生加成反应
(3)E与新制Cu(OH)2反应的化学方程式为 .
(4)G的同分异构体有多种,满足以下条件的同分异构体有种.
A.分子中含有环己烷的结构
B.能与NaHCO3溶液反应,放出气体
C.1mol该物质能与2molNa完全反应
(5)已知“Diels﹣Alder反应”为: ![]()
物质D与呋喃( ![]() )也可以发生“Diels﹣Alder反应”,该化学方程式为:
)也可以发生“Diels﹣Alder反应”,该化学方程式为:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对分子性质的解释中,不正确的是( )
A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
B.由于乳酸( ![]() )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体
)中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体
C.HF的稳定性很强,是因为其分子间能形成氢键
D.由图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子 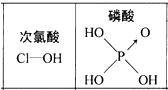
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用.
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7 , 其中1/3的Cu以罕见的Cu3+形式存在.Cu3+基态的核外电子排布式为
(2)磁性材料在生活和科学技术中应用广泛.研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性.下列物质适合做录音带磁粉原料的是(填选项字母).
A.V2O5
B.CrO2
C.PbO
D.ZnO
(3)屠呦呦因在抗疟药﹣﹣青蒿素(C15H22O5)研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人.青蒿素的结构简式如图l所示,碳原子的杂化方式为 . 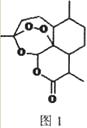
(4)“可燃冰因储量大”,污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃冰”结构如图2所示 
①“可燃冰”中分子间存在的2种作用力为
②H2O的键角大于CH4原因为
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,该电池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有个碳原子.已知石墨的层间距为a pm,C﹣C键长为b pm,阿伏伽德罗常数的值为NA , 则石墨晶体的密度为g.cm﹣3(列出计算式). 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钙固体登山运动员常用的能源提供剂.某兴趣小组长拟选用如图装置制备氢化钙. 
请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为(填仪器接口的字母编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞(请按正确的顺序填入下列步骤的标号).
A.加热反应一段时间
B.收集气体并检验其纯度
C.关闭分液漏斗活塞
D.停止加热,充分冷却
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此判断,上述实验确有CaH2生成.
①写出CaH2与水反应的化学方程式;②该同学的判断不正确,原因是
(4)请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保护环境已经成为人类的共识。人类应以可持续发展的方式使用资源,以合理的方式对废物进行处理并循环使用。下列做法不利于环境保护的是( )
A.发电场的煤脱硫处理
B.将煤转化为水煤气作燃料
C.回收并合理处理聚乙烯塑料废物
D.电镀废液经中和后直接排放
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com