
对有机物:
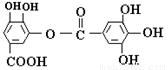
下列说法中不正确的是( )
(1)常温下,能与NaHCO3溶液反应放出CO2
(2)能发生碱性水解反应,1摩该有机物完全反应消耗掉8摩NaOH
(3)与稀H2SO4共热,生成2种有机物 (4)该有机物的分子式为C14H12O9
A.(1)(2) B.(3)(4) C.(1)(3) D.(2)(4)
科目:高中化学 来源: 题型:
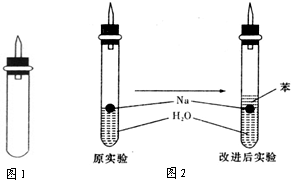 某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸;②Na+水;③Al+NaOH溶液.为点燃上述三个反应生成的H2,他们设计了如图所示的装置图:
某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸;②Na+水;③Al+NaOH溶液.为点燃上述三个反应生成的H2,他们设计了如图所示的装置图:查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸;②Na+水;③Al+NaOH溶液。为点燃上述三个反应生成的H2,他们设计了如右图所示的装置图:
![]()
]请回答下列问题:
(1)写出Al和NaOH溶液反应的离子方程式_______________________________。
(2)在点燃H2之前必须先进行____________________________________________。
(3)实验小组在点燃用上述装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量又太少。于是他们准备增加钠的用量,可教师说太危险,你认为产生危险的原因是___________________________。
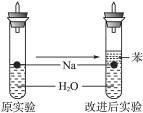
(4)实验小组查阅钠、苯(一种不溶于水的液态有机物)、水的密度分别为0.97 g·mL-1、0.88 g·mL-1、1.00 g·mL-1,并据此对实验进行了改进。在改进后的实验中H2的生成速率______________________。(填“减慢”或“加快”)
(5)2.3 g钠投入20 mL水中完全反应放出的气体在标准状况下的体积是_____________,所得溶液的物质的量浓度是______________________。(不计溶液体积的变化)
查看答案和解析>>
科目:高中化学 来源:2012年鲁科版高中化学选修6 4酿制米酒练习卷(解析版) 题型:填空题
乙醇是日常生活中最常见的有机物之一,乙醇的一种工业制法如下:
乙烯+A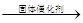 CH3CH2OH
CH3CH2OH
请回答下列问题:
(1)反应物乙烯的电子式为
________________________________________________________________________;
已知该反应中原子利用率为100%,符合绿色化学思想,则反应物A的化学式为________________。
(2)工业上还可以用硫酸为吸收剂的间接水合法合成乙醇,从对设备的影响和产品分离角度分析该法与固体催化剂法相比,缺点是
________________________________________________________________________。
(3)乙酸和乙醇在一定条件下可发生反应生成一种有香味的物质,该反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
该反应是可逆反应,请说出提高反应物转化率的一种方法:
________________________________________________________________________。
(4)固体酒精是一种便携的燃料,其中一种制备方法是将饱和醋酸钙溶液加入酒精中致使醋酸钙从酒精溶液中析出,呈半固态的凝胶状物质——“胶冻”,酒精填充其中,点燃胶状物时,酒精便燃烧起来。该过程说明醋酸钙在酒精中的溶解度________(填“大于”或“小于”)醋酸钙在水中的溶解度。
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
⑴(8分)甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验。
甲组:沉淀分析法
把一定量的混合物溶解后加入过量CaCl2,然后将所得沉淀过滤、洗涤、烘干、称量,所得固体是 (填化学式);写出该反应的离子方程式________________________ __。
 乙组:气体分析法
乙组:气体分析法
把一定量的混合物与足量盐酸反应后,用如图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是_________________,(将选项填入空格中)
A.氢氧化钠溶液 B.饱和氯化钠溶液 C.饱和碳酸氢钠溶液
选用该溶液后实验结果还是不准确,原因是_________________________________。
⑵(5分)某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:
① Zn+盐酸;② Na+水;③ Al+NaOH溶液。为点燃上述三个反应生成的H2,他们设计了如下图(原实验)所示的装置图,请回答下列问题:
①写出Al和NaOH溶液反应的化学方程式 。
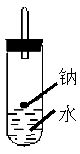
② 实验小组在点燃用此装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量又太少。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是 。
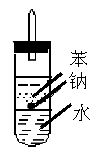
③ 实验小组查阅钠、苯(一种不溶于水的液态有机物)、水的密度分别为0.97g/mL、0.88g/mL、1.00g/mL,并据此对实验进行了改进。

在改进后的实验中H2的生成速率减慢。原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com