
| A. | NO3-、CO32-、SO42- | B. | NO3- | ||
| C. | SO32-、NO3- | D. | CO32-、NO3-、Na+ |
科目:高中化学 来源: 题型:选择题
| A. | 硅单质溶于入氢氧化钠溶液中:Si+2OH-+H2O═SiO3-+2H2↑ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至沉淀物质的量最多:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | 在碳酸氢镁溶液中加入过量氢氧化钠溶液:Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | |
| D. | 向NaAlO2溶液中加入过量稀盐酸:AlO2-+4H+═Al3++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
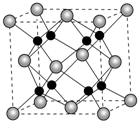 卤族元素中Cl、Br、I在海洋中含量丰富,F在自然界中常以CaF2的形式存在.
卤族元素中Cl、Br、I在海洋中含量丰富,F在自然界中常以CaF2的形式存在. ,1molNH4NO3中含有σ键数目为7mol(或7×6.02×1023).其中阴、阳离子中心原子杂化类型分别为:sp2、sp3.
,1molNH4NO3中含有σ键数目为7mol(或7×6.02×1023).其中阴、阳离子中心原子杂化类型分别为:sp2、sp3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有过渡元素都是金属元素 | |
| B. | CaO2和CaCl2含有的化学键类型完全相同 | |
| C. | 非金属原子之间不可能形成离子键 | |
| D. | 有化学键断裂的过程一定属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 有机化合物的结构简式可进一步简化,如:
有机化合物的结构简式可进一步简化,如: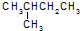 可简化为
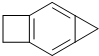
可简化为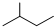 ,如图是一种形状酷似发射航天器的火箭的有机物分子(Rocketene),有关Rocketene的说法正确的是( )
,如图是一种形状酷似发射航天器的火箭的有机物分子(Rocketene),有关Rocketene的说法正确的是( )| A. | 该有机物属于烃的衍生物 | |
| B. | 该有机物属于苯的同系物 | |
| C. | Rocketene分子式为C9H8 | |
| D. | Rocketene与液溴用铁作催化剂反应生成的一溴代物有四种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
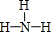 ;它的另一种氢化物R2H4是一种火箭燃料的成分,其电子式是
;它的另一种氢化物R2H4是一种火箭燃料的成分,其电子式是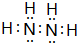 .
.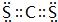 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
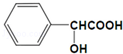
 +2Na→
+2Na→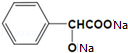 +H2↑.
+H2↑.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
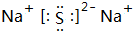 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com