
| 物质 名称 | 丁烷与 2--甲基丙烷 | 红磷 与白磷 | 庚烷与 十六烷 | 氕与 氘、氚 | 新戊烷与 2,2--二甲基丁烷 | 2--甲基戊烷与 2,3--二甲基丁烷 |
| 相互 关系 |
| 物质 名称 | 丁烷与 2--甲基丙烷 | 红磷 与白磷 | 庚烷与 十六烷 | 氕与 氘、氚 | 新戊烷与 2,2--二甲基丁烷 | 2--甲基戊烷与 2,3--二甲基丁烷 |
| 相互 关系 | ③ | ② | ④ | ① | ④ | ③ |


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
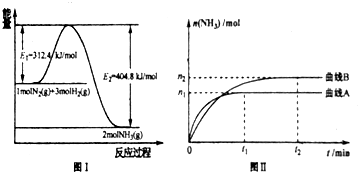
| n1 |
| 4t1 |
| 7 |
| 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某温度下,化学反应速率无论是用A、B、C何种物质来表示,其化学反应速率的数值相同 |
| B、在其他条件不变的情况下,降低温度,一般化学反应速率降低 |
| C、在其他条件不变的情况下,增大压强,单位体积内活化分子百分数一定增大,化学反应速率一定增大 |
| D、若增大或减少A物质的量,化学反应速率一定会发生明显的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
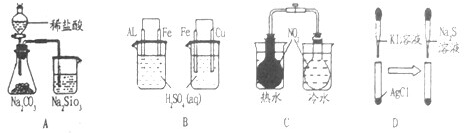
| 实验 | 实验现象 | 结论 |
| A | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
| B | 左烧杯铝表面冒气泡,右烧杯铜表面冒气泡 | 活动性:Al>Fe>Cu |
| C | 左烧瓶气体颜色加深,右烧瓶气体颜色变浅 | NO2转化为N2O4吸热 |
| D | 白色固体先变为黄色,后变为黑色 | 溶解度:AgCl>Agl>Ag2S |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.5×10-4 |
| B、0.015 |
| C、5.4×10-5 |
| D、无法计算 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com