
【化学--选修3物质结构与性质】(15分)
铜、铁都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。
请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下: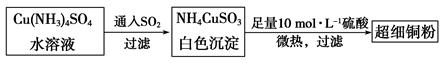
①Cu2+的价电子排布图 ; NH4CuSO3中N、O、S三种元素的第一电离能由大到小顺序为_______________________(填元素符号)。
②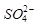 的空间构型为_____________,
的空间构型为_____________,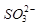 离子中心原子的杂化方式为 。
离子中心原子的杂化方式为 。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式: 。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是
a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成3种不同的氢键
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因 .
(4)Cu晶体的堆积方式如图所示,设Cu原子半径为r,
晶体中Cu原子的配位数为_______,晶体的空间利用率
为 ( 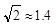 ,列式并计算结果)。
,列式并计算结果)。
(15分)
(1)① 
N>O>S (1分)
②正四面体形(1分)sp3杂化(1分)
(2) 2Cu(NH3)42++3SO2+4H2O=2NH4CuSO3↓+6NH4++SO42-(2分)
(3)① c(1分) ②乙醇分子极性比水分子极性弱,加入乙醇降低溶剂的极性,从而减小溶质的溶解度(2分) 
(4)12 (2分)  或
或 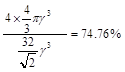 或
或  ( 或 74.8%,列式2分,结果1分,共3分)
( 或 74.8%,列式2分,结果1分,共3分)
解析试题分析:(1)①Cu2+的价层电子数是9个,所以Cu2+的价电子排布图为 ;N、O、S三种元素中由于N原子的2p轨道是半充满状态,所以第一电离能最大;同主族元素,随电子层数的增多,第一电离能逐渐减小,所以3种元素的第一电离能由大到小顺序为N>O>S
;N、O、S三种元素中由于N原子的2p轨道是半充满状态,所以第一电离能最大;同主族元素,随电子层数的增多,第一电离能逐渐减小,所以3种元素的第一电离能由大到小顺序为N>O>S
②SO42-的价层电子对数=4+1/2(6+2-4×2)=4,所以空间构型为正四面体型;SO32-离子的价层电子对数=3+1/2(6+2-3×2)=4,所以中心原子的杂化方式为sp3杂化;
(2)由流程图可知向Cu(NH3)4SO4水溶液中通入SO2时生成白色沉淀,根据所给沉淀的化学式书写离子方程式,所以离子方程式为2Cu(NH3)42++3SO2+4H2O=2NH4CuSO3↓+6NH4++SO42-;
(3)①a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成2种不同的氢键,N与H,O与H之间,错误;b.NH3分子和H2O分子,分子空间构型不同,氨气是三角锥型,水是角形,氨气分子的键角大于水分子的键角,错误;c. Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键,硫酸根离子与配离子之间是离子键,N与H之间是共价键,氨气与铜离子之间是配位键,正确;d. Cu(NH3)4SO4组成元素中电负性最大的是氧元素,错误,答案选c;
②根据相似相容原理,极性分子易溶于极性溶剂,乙醇分子极性比水分子极性弱,加入乙醇降低溶剂的极性,从而减小溶质的溶解度;
(4)Cu晶体的堆积方式是面心立方最密堆积,所以配位数是12;由图可知,立方体的面的对角线长是4r,所以立方体的棱长a=2 r,1个Cu的体积是4/3πr3,晶胞中Cu原子的个数是4个,所以晶体的空间利用率为4×4/3πr3/a3=
r,1个Cu的体积是4/3πr3,晶胞中Cu原子的个数是4个,所以晶体的空间利用率为4×4/3πr3/a3= .
.
考点:考查电子排布图的书写,元素第一电离能的判断,空间构型、杂化轨道的判断,化学键类型的判断,.离子方程式的书写,晶胞的计算


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:填空题
叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为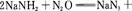
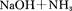
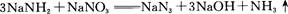 回答下列问题:
回答下列问题:
(1)氮所在的周期中,电负性最大的元素是 ,第一电离能最小的元素是 。
(2)基态氮原子的L层电子排布图为 。
(3)与N3-互为等电子体的分子为 (写出一种)。依据价层电子对互斥理论,NO3-的空间构型为 。
(4)氨基化钠(NaNH2)和叠氮化钠(NaN3)的晶体类型为 。叠氮化钠的水溶液呈碱性,用离子方程式表示其原因: 。
(5)N20沸点(一88.49℃比NH3沸点(一33.34℃)低,其主要原因是
(6)安全气囊的设计原理为
①氮分子中δ键和π键数目之比为 。
②铁晶体中存在的化学键类型为 。
③铁晶体为体心立方堆积,其晶胞如图所示,晶胞边长为a cm,该铁晶体密度为
(用含a、NA的表达式表示,其中NA为阿伏加德罗常数)。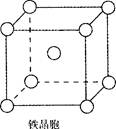
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(15分)已知A、B、C、D四种短周期元素,它们的核电荷数依次增大。A原子、C原子的L能层中,都有两个未成对的电子,C、D同主族。 E、F都是第四周期元素,E原子核外有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
⑴基态D原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 ;
⑵E2+离子的价层电子排布图是 ,F原子的电子排布式是 ;
⑶A元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为 , B元素的气态氢化物的VSEPR模型为 ;
⑷化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的电子式为 ;
⑸配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6,甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程式为 ;
⑹某种化合物由D,E,F三种元素组成,其晶胞如图所示,则其化学式为 ,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度:
d= g/cm3。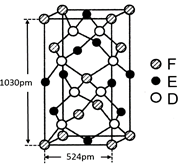
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分,每空2分)氮化钠(Na3N)是科学家制备的一种重要化合物,它与水作用可产生NaOH和NH3。请回答下列问题:
(1)Na3N的电子式是_______;该化合物是由______键形成的_____(填“离子”或“共价”)化合物。
(2)Na3N与盐酸反应生成__________种盐,对应的反应方程式是 。
(3)比较Na3N中两种微粒的半径:r(Na+)__________r(N3-)(填“>”“=”“<”符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(16分)X、Y、Z、W是常见的四种短周期元素,其原子序数依次增大。其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子最外层电子排布式为nsnnpn |
| Y | Y是空气中含量最高的元素 |
| Z | Z是地壳中含量最高的金属元素 |
| W | W的单质是常见的半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。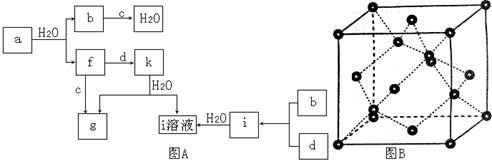
回答下列问题:
(1)图B对应的物质名称是 ,其晶胞中的原子数为 ,晶体的类型为 。
(2)d中元素的原子核外电子排布式为 。
(3)图A中由二种元素组成的物质中,沸点最高的是 ,原因是 ,该物质的分子构型为 ,中心原子的杂化轨道类型为 。
(4)图A中的双原子分子中,极性最大的分子是 。
(5)k的分子式为 ,中心原子的杂化轨道类型为 ,属于 分子(填“极性”或“非极性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D代表元素周期表中4种元素,请完成下列问题
(1)A元素的基态原子的最外层有3个未成对电子,次外层有2个电子,该元素氢化物比同族元素氢化物熔沸点高的原因是 ;第一电离能比后面一号元素大的原因是
(2)B元素与氧元素形成的一种化合物是含有4个原子18个电子的分子,该化合物的电子式为 ,若向该化合物的稀溶液中加入少量二氧化锰,有无色气体产生,该反应的化学方程式为
(3)C元素的正三价离子的 3d轨道为半充满状态,C元素的符号为 ,在同期表中位于 周期 族,原子结构示意图为
(4)D元素位于元素周期表第四周期第ⅠB族,其基态原子的电子排布式为
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)写出氯原子的原子结构示意图
(2)氯元素的原子在反应中易 (填“得”或“失”) 个电子,表现出 性。
(3)氯元素的最高化合价为 ,最低化合价为 。
(4)氯元素的非金属性 (填“强”或“弱”)于硫元素的非金属性。
(5)写出氯元素、硫元素最高价氧化物对应水合物的化学式并比较酸性强弱 。
(6)请写出下列物质的电子式。NaCl H2O CO2 N2 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
(1)在这10种元素中,非金属性最强的是 (填序号);
(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为 ,元素②与⑨形成的18e-化合物的电子式 ;
(3)②⑨⑩三种元素形成的化合物M中原子个数比为3:4:2,电子总数为42,M中含有的化学键类型有 ;
(4)比较元素⑦⑧形成的气态氢化物的稳定性: > (用化学式表示)
(5)元素⑤的氧化物与氢氧化钠溶液反应的离子方程式 。
(6)元素④和③形成的化合物属于 化合物,用电子式表示其形成过程 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com