
 ��
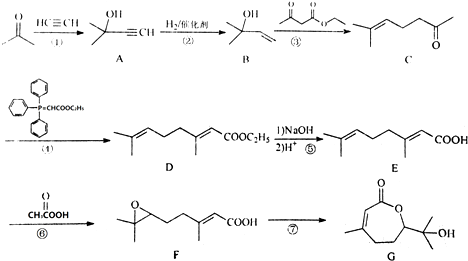
��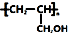 ��д���ϳ�����ͼ�����Լ����ã����ϳ�����ͼʾ�����£�CH2=CH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH��
��д���ϳ�����ͼ�����Լ����ã����ϳ�����ͼʾ�����£�CH2=CH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH�� ���� ��1��C�к���̼̼˫�����ʻ�������G�Ľṹ��ʽȷ�������ʽ��
��2���Ա����ʵĽṹ��֪����Ӧ��Ϊ�ӳɷ�Ӧ����Ӧ6��E��̼̼˫��������һ�������Ѽ���������������Ӧ��
��3����Ӧ�ٻ���õ���һ����H�������ʽΪC8H14O2��2���ӱ�ͪ����Ȳ�����ӳɷ�Ӧ��
��4��E��������ᷴӦ�õ�F�����غ��֪���������
��5��һ����G��ȥһ����ˮ�ɵ�����J��J�ķ���ʽΪC10H14O2�������Ͷ�Ϊ$\frac{2��10+2-14}{2}$=4��J��ͬ���칹����ϣ�������FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ����ɲ����Ͷȿ�֪������û�в����ͼ����ڱ����ϵ�ȡ������2�ֹ�4���������Ϊ2��-CH2CH3��2��-OH��
��6���״��������ɼ�ȩ����ȩ����Ȳ�����ӳɷ�Ӧ�õ�HC��CCH2OH���������������ӳɷ�Ӧ�õ�CH2=CHCH2OH��������Ӿ۷�Ӧ�õ�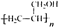 ��
��
��� �⣺��1����C�Ľṹ��ʽ��֪�����еĹ�������̼̼˫�����ʻ�������G�Ľṹ��ʽ����֪�����ʽΪC10H16O3��
�ʴ�Ϊ��̼̼˫�����ʻ���C10H16O3��
��2���Ա����ʵĽṹ��֪����Ӧ��Ϊ�ӳɷ�Ӧ����Ӧ6��E��̼̼˫��������һ�������Ѽ���������������Ӧ��
�ʴ�Ϊ���ӳɷ�Ӧ��������Ӧ��
��3����Ӧ�ٻ���õ���һ����H�������ʽΪC8H14O2��2���ӱ�ͪ����Ȳ�����ӳɷ�Ӧ���ṹ��ʽΪ��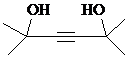
�ʴ�Ϊ��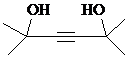
��4��E��������ᷴӦ�õ�F�����غ��֪������CH3COOH��
�ʴ�Ϊ��CH3COOH��
��5��һ����G��ȥһ����ˮ�ɵ�����J��J�ķ���ʽΪC10H14O2�������Ͷ�Ϊ$\frac{2��10+2-14}{2}$=4��J��ͬ���칹����ϣ�������FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ����ɲ����Ͷȿ�֪������û�в����ͼ����ڱ����ϵ�ȡ������2�ֹ�4���������Ϊ2��-CH2CH3��2��-OH�������һ�����ʱ��2��-OH��4��λ�ã������һ����ʱ��2��-OH��4��λ�ã������һ����ʱ��2��-OH��3��λ�ã��ʷ���������ͬ���칹�干��11�֣�
�ʴ�Ϊ��11��
��6���״��������ɼ�ȩ����ȩ����Ȳ�����ӳɷ�Ӧ�õ�HC��CCH2OH���������������ӳɷ�Ӧ�õ�CH2=CHCH2OH��������Ӿ۷�Ӧ�õ�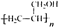 ���ϳ�·������ͼΪ��
���ϳ�·������ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л���ĺϳɡ������š��л���Ӧ���͡���������ͬ���칹����д�ȣ���5����ͬ���칹�����дΪ�״��㡢�ѵ㣬�Ƕ��л���ѧ���ۺϿ��飮


 ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
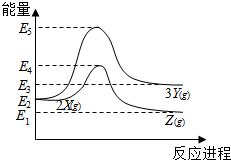
| A�� | ��X��Y��Ӧ�ġ�H=E5-E2 | B�� | ��X��Z��Ӧ�ġ�H��0 | ||
| C�� | ����ѹǿ���������Y�IJ��� | D�� | �����¶����������Z�IJ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
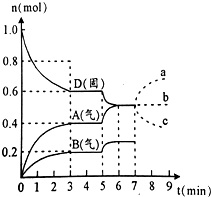 ���ݻ�Ϊ2.0L���ܱ������ڣ�����D��T��ʱ������Ӧ���䷴Ӧ�������������ʵ�����ʱ��t�ı仯��ϵ��ͼ����������������ǣ�������
���ݻ�Ϊ2.0L���ܱ������ڣ�����D��T��ʱ������Ӧ���䷴Ӧ�������������ʵ�����ʱ��t�ı仯��ϵ��ͼ����������������ǣ�������| A�� | �ӷ�Ӧ��ʼ����һ�δﵽƽ��ʱ��A���ʵ�ƽ����Ӧ����Ϊ0.067mol/��L•min�� | |
| B�� | ������ͼ�÷�Ӧ��ƽ�ⳣ������ʽΪk=c2��A��•c��B�� | |
| C�� | ���ڵ�5����ʱ�����¶ȣ���÷�Ӧ������Ӧ�����ȷ�Ӧ����Ӧ��ƽ�ⳣ������B�ķ�Ӧ�������� | |
| D�� | ���ڵ�7����ʱ����D�����ʵ�����A�����ʵ����仯�������a���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ��������X��Y��Z��W | |
| B�� | ���Ӱ뾶��W��X��Z | |
| C�� | W�ֱ���Y��Z�γɵĻ������л�ѧ�����Ͳ�ͬ | |
| D�� | ��̬�⻯����ȶ��ԣ�W��Y |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
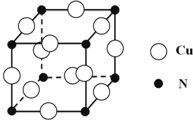 ��͵�Ԫ���ڻ�ѧ���к���Ҫ�ĵ�λ���ش��������⣺
��͵�Ԫ���ڻ�ѧ���к���Ҫ�ĵ�λ���ش��������⣺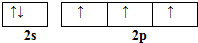 ��Ԥ����2017�귢��ġ��϶���š�̽�������õij���5�����ػ��ȼ��Ϊƫ������[��CH3��2NNH2]����CH3��2NNH2��Nԭ�ӵ��ӻ���ʽΪsp3��
��Ԥ����2017�귢��ġ��϶���š�̽�������õij���5�����ػ��ȼ��Ϊƫ������[��CH3��2NNH2]����CH3��2NNH2��Nԭ�ӵ��ӻ���ʽΪsp3��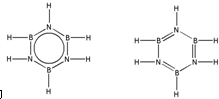 ����
�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
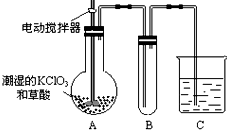 �ö������ȣ�CLO2������������ Na2FeO4Ħ������Ϊ166g•mol-1������
�ö������ȣ�CLO2������������ Na2FeO4Ħ������Ϊ166g•mol-1�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ԫ����Ԫ�����ڱ��е���������W=X��Y��Z | |
| B�� | ����������Ӧ��ˮ��������ԣ�W��Z | |
| C�� | ���Ӱ뾶��X��Y��Z | |
| D�� | YW3������NaOH��Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
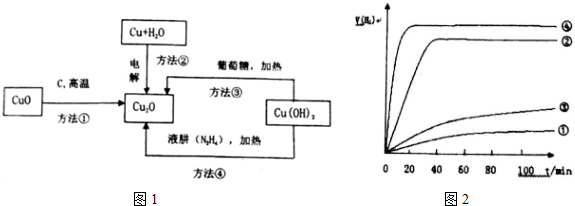
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com