
| A. | 反应Ⅰ中S单质是氧化剂 | |
| B. | 反应ⅡAl2O3中Al元素被氧化 | |
| C. | 当生成5.4 g Al时,反应Ⅰ和反应Ⅱ共转移1.2 mol e- | |
| D. | 反应Ⅰ氧化产物与还原产物物质的量之比为2:9 |
分析 反应I:2Al2(SO4)3+3S$\frac{\underline{\;高温\;}}{\;}$2Al2O3+9SO2↑中,S元素的化合价由+6价降低为+4价,S元素的化合价由0升高为+4价;
反应Ⅱ:2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑中,Al元素的化合价降低,O元素的化合价升高,以此来解答.
解答 解:A.反应Ⅰ中S单质是还原剂,故A错误;
B.反应ⅡAl2O3中Al元素得到电子被还原,故B错误;
C.当生成5.4 g Al时,n(Al)=0.2mol反应Ⅰ和反应Ⅱ共转移电子为0.1mol×$\frac{12}{2}$+0.1mol×6=1.2 mol e-,故C正确;
D.反应Ⅰ氧化产物与还原产物均为SO2,由S原子守恒可知,物质的量之比为3:6=1:2,故D错误;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意转移电子的计算及基本概念的应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
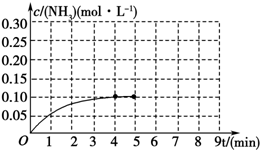 在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0 反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题:
在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0 反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解、过滤、加热(升华)、蒸发(结晶) | B. | 加热(升华)、溶解、过滤、蒸发(结晶) | ||
| C. | 升华、溶解、蒸馏、结晶 | D. | 溶解、结晶、过滤、升华 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减小C或D的浓度 | B. | 减小B的浓度 | C. | 增大A或B的浓度 | D. | 减小A的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量的铜与浓硝酸反应能产生NO | |
| B. | 将CO2、SO2通入Ca(ClO)2溶液均发生反应且反应类型相同 | |
| C. | SiO2与所有的酸都不能发生反应 | |
| D. | 加过量盐酸产生能使澄清石灰水变浑浊气体的钠盐为Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下将pH=2的硫酸和pH=12的MOH溶液等体积混合,所得溶液pH≤7 | |
| B. | 已知同温度相同浓度的NaNO2溶液比NaF溶液的碱性强,所以氢氟酸的酸性比亚硝酸的弱 | |
| C. | 常温下,将醋酸钠、盐酸两溶液混合后,溶液呈中性,则有c(Na+)>c(Cl-)=c(CH3COOH) | |
| D. | pH相等的NH4Cl、(NH4)2SO4、NH4HSO4三种溶液物质的量浓度为c(NH4Cl)>c((NH4)2SO4)=c(NH4HSO4) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com