
 .
.分析 短周期主族元素W、R、X、Y、Z的原子序数依次增大,且分别占三个不同的周期,则W应为H元素,W与X同主族,则X为Na元素,R最外层电子数是其内层电子数的3倍,则R为O元素,R与Z同主族,则Z为S元素,Y是地壳中含量最多的金属元素,则Y为Al元素,据此答题.
解答 解:短周期主族元素W、R、X、Y、Z的原子序数依次增大,且分别占三个不同的周期,则W应为H元素,W与X同主族,则X为Na元素,R最外层电子数是其内层电子数的3倍,则R为O元素,R与Z同主族,则Z为S元素,Y是地壳中含量最多的金属元素,则Y为Al元素,
(1)根据元素周期律可知,H、O、Na、Al、S五种元素中金属性最强的元素是Na,
故答案为:Na;
(2)电子层数越多,半径越大,电子层数相同时,核电荷数越多,半径越小,所以O、Al、S的原子半径由大到小的顺序是Al>S>O,
故答案为:Al>S>O;
(3)W2R为H2O,H2O中含有的化学键类型为共价键,
故答案为:共价键;
(4)Z为S元素,Z原子的结构示意图为  ,故答案为:
,故答案为: ;
;
(5)五种元素的单质中,Na能与氢氧化钠溶液中的水生成氢气也能与盐酸生成氢气,Al既能与盐酸反应生成H2又能与氢氧化钠溶液反应生成H2,
故答案为:Na、Al.
点评 本题考查了元素位置结构性质的判断,题目难度不大,熟悉元素周期表结构是解本题关键,根据原子结构来推断元素,再结合物质的结构、性质来分析解答.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:选择题
| A. | 16g O2中含有的氧分子数为NA | |
| B. | 1mol Zn变为Zn2+时失去的电子数目为NA | |
| C. | 常温常压下,11.2 L H2中含有的氢分子数为0.5NA | |
| D. | 1L 1 mol•L-1 BaCl2溶液中含有的钡离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂可加快SO2转化为SO3的速率 | |
| B. | H2、I2、HI平衡混合气加压后颜色变深 | |
| C. | 装有NO2、N2O4平衡混合气的玻璃球在冷水中气体颜色变浅 | |
| D. | SO2通入氯水,氯水的颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | |
| B. | H2C=CH2+Br2→CH3CHBr | |
| C. |  | |
| D. | CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3CH2CH3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应可能是吸热反应也可能是放热反应 | |
| B. | 1 mol强酸与1mol强碱发生中和反应所放出的热量叫做中和热 | |
| C. | 二次电池充电时将电能转化为化学能 | |
| D. | 催化剂表面做成蜂窝状更有利于提高催化效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
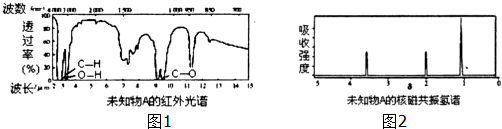
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
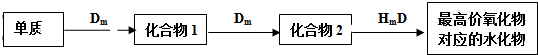
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,含有离子键和共价键(填化学键类型),属于离子化合物 (填“离子化合物”或“共价化合物”)
,含有离子键和共价键(填化学键类型),属于离子化合物 (填“离子化合物”或“共价化合物”)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com