
| A£® | HCl | B£® | BaCl2 | C£® | NaOH | D£® | AgNO3 |
·ÖĪö ČżÖÖĪļÖŹŗ¬ÓŠµÄŃōĄė×Ó²»Ķ¬£¬ĘäÖŠAlCl3”¢MgSO4¶¼æÉÓė¼ī·“Ӧɜ³É³Įµķ£¬µ«¼ī¹żĮæŹ±£¬ĒāŃõ»ÆĀĮæÉČÜÓŚĒæ¼ī£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA£®¼ÓČėŃĪĖį£¬¶¼²»·“Ó¦£¬²»Äܼų±š£¬¹ŹA“ķĪó£»
B£®¼ÓČėĀČ»Æ±µ£¬¶¼Éś³É³Įµķ£¬²»Äܼų±š£¬¹ŹB“ķĪó£»
C£®¼ÓČėĒāŃõ»ÆÄĘČÜŅŗ£¬Na2SO4”¢AlCl3”¢MgSO4ČżÖÖČÜŅŗĻÖĻó·Ö±šĪŖ£ŗĪŽĻÖĻó”¢ĻČÉś³É³ĮµķŗóČܽā”¢Éś³É°×É«³Įµķ£¬æɼų±š£¬¹ŹCÕżČ·£»
D£®¼ÓČėĻõĖįŅųČÜŅŗ£¬¶¼Éś³É³Įµķ£¬²»Äܼų±š£¬¹ŹD“ķĪó£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ¼ģŃéŗĶ¼ų±š£¬ĪŖøßĘµæ¼µćŗĶ³£¼ūĢāŠĶ£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶŹµŃéÄÜĮ¦µÄ漲飬עŅā°ŃĪÕĪļÖŹµÄŠŌÖŹµÄŅģĶ¬£¬ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬Ķ¬Ź±×¢Ņā°ŃĪÕŹµŃéµÄŗĻĄķŠŌŗĶæÉŠŠŠŌµÄĘĄ¼Ū£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĖįŠŌŃõ»ÆĪļ²»Ņ»¶Ø¶¼ÄÜÓėĖ®·“Ӧɜ³ÉĖį | |
| B£® | ijČÜŅŗ¼ÓČėŃĪĖįĖį»ÆµÄBaCl2ČÜŅŗ²śÉś°×É«³Įµķ£¬ŌņŌČÜŅŗÖŠŗ¬ÓŠSO42- | |
| C£® | ¶”“ļ¶ūŠ§Ó¦æÉŅŌÓĆÓŚĒų±šFeCl3ČÜŅŗŗĶFe£ØOH£©3½ŗĢå | |
| D£® | ĻÖ“ś»Æѧ·ÖĪö²āŹŌ³£½čÖśŅ»Š©ŅĒĘ÷Ą“·ÖĪöĪļÖŹ×é³É£¬ČēÓĆŌ×ÓĪüŹÕ¹āĘ×Č·¶ØĪļÖŹÖŠŗ¬ÓŠÄĒŠ©½šŹōŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
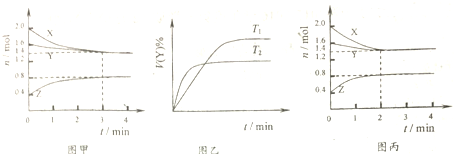
| A£® | T1”ꏱ£¬ČŻĘ÷ÖŠ·¢ÉśµÄ·“Ó¦æɱķŹ¾ĪŖ£ŗ3X£Øg£©+Y£Øg£©?2Z£Øg£©£¬ĒŅÕż·“Ó¦·ÅČČ | |
| B£® | T1”ꏱ£¬·“Ó¦½ųŠŠµÄĒ°3minÄŚ£¬ÓĆX±ķŹ¾µÄ·“Ó¦ĖŁĀŹv£ØX£©=0.2mol•£ØL•min£©-1 | |
| C£® | T1”ꏱ£¬3min“ļµ½Ę½ŗāŗó£¬ĻņČŻĘ÷ÖŠŌŁ¼ÓČė2.0mol X”¢1.6mol Y”¢0.4mol Z£¬·“Ó¦“ļµ½ŠĀĘ½ŗāŹ±£ŗ0.7mol•L-1£¼c£ØY£©£¼1.4mol•L-1 | |
| D£® | Čōøı䷓ӦĢõ¼ž£¬Ź¹·“Ó¦½ų³ĢČēĶ¼±ūĖłŹ¾£¬ŌņøıäµÄĢõ¼žŹĒŹ¹ÓĆ“ß»Æ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
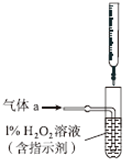 ĮņĖį¹¤Ņµ²śÉśµÄ·ĻĘų£ØÖ÷ŅŖ³É·Ö£ŗSO2”¢O2”¢N2”¢CO2µČ£©Åŷŵ½æÕĘųÖŠ»įĪŪČ¾»·¾³£®Ä³»ÆѧŠĖȤŠ”×é¶Ō·ĻĘųµÄ×é³É½ųŠŠĢ½¾æ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ĮņĖį¹¤Ņµ²śÉśµÄ·ĻĘų£ØÖ÷ŅŖ³É·Ö£ŗSO2”¢O2”¢N2”¢CO2µČ£©Åŷŵ½æÕĘųÖŠ»įĪŪČ¾»·¾³£®Ä³»ÆѧŠĖȤŠ”×é¶Ō·ĻĘųµÄ×é³É½ųŠŠĢ½¾æ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
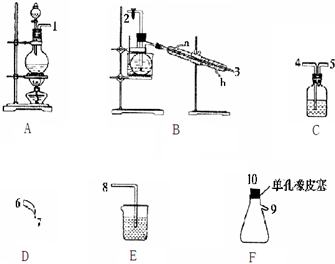
| ĪļĄķŠŌÖŹ | ÖʱøŌĄķ | »ÆѧŠŌÖŹ |
| »ĘÉ«ÓĶדŅŗĢå ČŪµćĪŖ-40”ę£¬·ŠµćĪŖ71”ę ²»ČÜÓŚĄäĖ®£¬Ņ×ČÜÓŚÓŠ»śČܼĮ ĆܶČĪŖ1.65g/mL | Cl2ÓėNH4ClĖ®ČÜŅŗŌŚµĶĪĀĻĀ·“Ó¦ | 95”걬ÕØ£¬ČČĖ®ÖŠ·¢ÉśĖ®½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

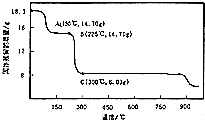
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
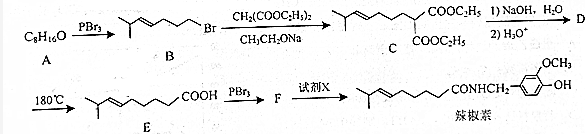
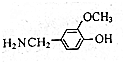 £¬ÓÉB”śCµÄ·“Ó¦ĄąŠĶŹĒČ”“ś£¬
£¬ÓÉB”śCµÄ·“Ó¦ĄąŠĶŹĒČ”“ś£¬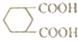 µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£¬ÉĻŹöĮ÷³ĢÖŠ³öĻֵďŌ¼ĮæÉÓĆ£©£®ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾ĄżČēĻĀ£ŗCH2=CH2$\stackrel{HBr}{”ś}$^CH3CH2Br$”ś_{”÷}^{NaOHČÜŅŗ}$CH3CH2OH£®
µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£¬ÉĻŹöĮ÷³ĢÖŠ³öĻֵďŌ¼ĮæÉÓĆ£©£®ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾ĄżČēĻĀ£ŗCH2=CH2$\stackrel{HBr}{”ś}$^CH3CH2Br$”ś_{”÷}^{NaOHČÜŅŗ}$CH3CH2OH£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±½µÄŅ»ŌŖČ”“śĪļƻӊĶ¬·ÖŅģ¹¹Ģå | B£® | ±½µÄĮŚĪ»¶žŌŖČ”“śĪļÖ»ÓŠŅ»ÖÖ | ||
| C£® | ±½µÄ¼äĪ»¶žŌŖČ”“śĪļÖ»ÓŠŅ»ÖÖ | D£® | ±½µÄ¶ŌĪ»¶žŌŖČ”“śĪļÖ»ÓŠŅ»ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ĀČ»Æļ§ČČ·Ö½ā·“Ó¦ | B£® | µŖĘųŗĶĒāĘų»ÆŗĻÉś³É°±µÄ·“Ó¦ | ||
| C£® | µāÉż»Ŗ | D£® | ĀĢÉ«Ö²ĪļµÄ¹āŗĻ×÷ÓĆÉś³Éµķ·Ū |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com