
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是_____、_______杂化轨道分别是________、_________;a分子的立体结构是____________。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______晶体、_______晶体:
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)__________;
(4)Y与Z比较,电负性较大的____________, 其+2价离子的核外电子排布式是_________。
该题是否有问题?题干中提到了W,但问题中并未涉及。
答案:(1)CH4 SiH4 sp3 sp3 正四面体
(2)分子 原子
(3)CO2
(4)C 1s22s2
解析:由“Y原子的L层p轨道中有2个电子”可知Y原子的电子排布式是1s22s22p2,为碳元素;由“Z与Y原子的价层电子数相同”可知Z与碳元素同主族,又因Z位于元素周期表的前四周期且核电荷数大于Y,所以Z可能为硅元素(14号)或锗元素(32号),若Z为锗元素,则四种元素的核电荷数之和大于51(因W的核电荷数比Z的还要大),即Z只能为硅元素;由“W原子的L层电子数与最外层电子数之比为41”可知W的最外层电子数为2,由“d轨道中的电子数与最外层电子数之比为51”可知d轨道中的电子数为10,所以W原子的电子排布式是1s22s22p63s23p63d104s2,即W为锌元素;又因四种元素的核电荷数之和为51,所以X元素的核电荷数为1,是氢元素。


科目:高中化学 来源: 题型:

(1)该反应是____________________反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率______(填“增大”“减小”“不变”),
原因是____________________________________________;
(3)反应体系中加入催化剂对反应热是否有影响?_______________,原因是_________:
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”“减小、”“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年海南卷)(8分)反应A(g)+B(g) ![]() C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
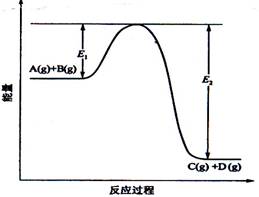
(1)该反应是____________________反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率______(填“增大”“减小”“不变”),
原因是____________________________________________;
(3)反应体系中加入催化剂对反应热是否有影响?_______________,原因是_________:
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”“减小、”“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年海南卷)(10分)A、B、C、D、E均为有机化合物,它们之间的关系如图所示(提示:RCH=CHR'在酸性高锰酸钾溶液中反应生成RCOOH和R'COOH,其中R和R'为烷基)。

回答下列问题:
(1)直链化合物A的相对分子质量小于90,A分子中碳、氢元素的总质量分数为0.814,其余为氧元素,则A的分子式为_____________;
(2)已知B与NaHCO3溶液完全反应,其物质的量之比为1:2,则在浓硫酸的催化下,B与足量的C2H5OH发生反应的化学方程式是___ 反应类型为_____:
(3)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是__________________
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有__________种,其相应的结构简式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年海南卷)(11分)如何防止铁的锈蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
序号 | 内容 | 实验现象 |
1 | 常温下将铁丝放在干燥空气中一个月 | 干燥的铁丝表面依然光亮 |
2 | 常温下将铁丝放在潮湿空气中一小时 | 铁丝表面依然光亮 |
3 | 常温下将铁丝放在潮湿的空气中一个月 | 铁丝表面已变得灰暗 |
4 | 将潮湿的铁丝放在常温的氧气流中一小时 | 铁丝表面略显灰暗 |
5 | 将潮湿的铁丝放在高于常温的氧气流中一小时 | 铁丝表面已变得灰暗 |
6 | 将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时 | 铁丝表面灰暗程度比实验5严重 |
回答以下问题:
(1)上述实验中发生了电化学腐蚀的是(填实验序号) __________; 在电化学腐蚀中,负极反应是________________; 正极反应是_______________________;
(2)由该实验可知,可以影响铁锈蚀速率的因素是_________________________;
(3)为防止铁的锈蚀,工业上普遍采用的方法是______________(答两种方法)
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年海南卷)锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为( )
A. 2mol B. 1 mol C. 0.5mol D. 0.25mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com