
在盛有KI溶液的试管中,滴入氯水充分反应后,再加入四氯化碳振荡,静置后观察到的现象是( )
A.上层紫红色,下层近无色
B.均一、透明、紫红色
C.均一、透明、无色
D.上层近无色,下层紫红色
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
元素的原子结构决定其性质和周期表中的位置。下列说法正确的是( )
A.元素原子的最外层电子数等于元素的最高化合价
B.多电子原子中,在离核较近的区域内运动的电子能量较高
C.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强
D.元素周期表中位于金属和非金属的分界线附近的元素属于过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,SiO2表现什么化学性质,在A~D选项中选出正确答案。
(1)SiO2+Na2CO3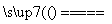 Na2SiO3+CO2↑______
Na2SiO3+CO2↑______
(2)SiO2+2C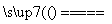 Si+2CO↑________
Si+2CO↑________
(3)SiO2+4HF===SiF4↑+2H2O________
A.作为玻璃的成分与氢氟酸反应而使玻璃能被雕刻
B.将挥发性的酸酐从其盐中代换出来
C.弱氧化性
D.强酸制弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中A、B、C、D分别代表有关反应中的一种化合物。其中物质A是一种高熔点化合物,不溶于硫酸、硝酸,却溶于氢氟酸。请填写以下空白:
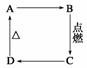
(1)A、B、C、D的化学式分别是________、________、________、________。
(2)A→B的化学方程式:________________________________________________
________________________________________________________________________。
(3)C→D的离子方程式:_________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
溴与氯的单质在性质上具有很大的相似性,但Cl2比Br2的活泼性强,下面是根据氯气的性质,对溴单质性质的预测,其中不正确的是( )
A.溴单质可以和烧碱溶液反应
B.溴单质只具有氧化性
C.在化学反应中可得1个电子,显-1价
D.可用硝酸酸化的AgNO3溶液来检验Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:



(1)指出提取碘的过程中有关的实验操作名称:
①____________;③____________;
写出实验②中有关反应的离子方程式:____________________________________。
(2)提取碘的过程中,可供选择的有关试剂是____。
A.酒精 B.四氯化碳
C.汽油 D.乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
北京奥运会开幕式在李宁点燃鸟巢主火炬时达到高潮。奥运火炬采用的是环保型燃料——丙烷,其燃烧时发生反应的化学方程式为C3H8+5O2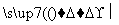 3CO2+4H2O。下列说法中不正确的是( )
3CO2+4H2O。下列说法中不正确的是( )
A.火炬燃烧时化学能只转化为热能
B.所有的化学反应都会伴随着能量变化,有能量变化的物质变化不一定是化学反应
C.1 mol C3H8和5 mol O2所具有的总能量大于3 mol CO2和4 mol H2O所具有的总能量
D.丙烷完全燃烧的产物对环境无污染,故丙烷为环保型燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L盐酸和20.00 mL 0.1000 mol/L醋酸溶液,得到2条滴定曲线,如下图所示:
以HA表示酸,下列说法正确的是
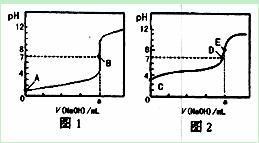
A.滴定盐酸的曲线是图2
B.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A—)
C.达到B、E状态时,反应消耗的n( CH3COOH)>n(HCl)
D.当0mL< V(NaOH)<20.00mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇可作为燃料电池的原料。工业上利用CO2和H2在一定条件下反应合成甲醇。
(1)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: 。
(2)甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
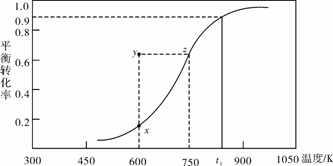
①600K时,Y点甲醇的υ(逆) (正)(填“>”或“<”)
②从Y点到X点可采取的措施是______________________________________。
③有同学计算得到在t1K时,该反应的平衡常数为8.1mol·L-1。你认为正确吗?请说明理由 。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。在相同的密闭容器中,使用不同方法制得的Cu2O(Ⅰ)和(Ⅱ)分别进行催化CH3OH的脱氢实验:CH3OH(g) HCHO(g)+H2(g)
HCHO(g)+H2(g)
CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
可以判断:实验①的前20 min的平均反应速率 ν(H2)= ;实验温度
T1 T2(填“>”、“<”);催化剂的催化效率:实验① 实验②(填“>”、“<”)。
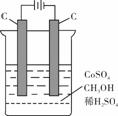 (4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如下图所示装置模拟上述过程,则Co2+在阳极的电极反应式为 ;除去甲醇的离子方程式为 。
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如下图所示装置模拟上述过程,则Co2+在阳极的电极反应式为 ;除去甲醇的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com