
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.40 | 20.38 |
| 第二次 | 25.00 | 4.00 | 24.02 |
分析 (1)根据滴定终点,锥形瓶中的溶液从红色变为无色时,且半分钟内不褪色,应停止滴定;
(2)根据待测溶液润洗锥形瓶,会使的待测液的物质的量增多;根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析误差;
(3)根据酸式滴定管用蒸馏水洗净后,应用标准液润洗;
(4)根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$计算,V(标准)用两次的平均值.
解答 解:(1)因滴定终点时,锥形瓶中的溶液从红色变为无色时,且半分钟内不褪色,停止滴定;故答案为:粉红色变为无色且在半分钟内不恢复;
(2)根据待测溶液润洗锥形瓶,会使的待测液的物质的量增多,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$,可知c(标准)偏大,故答案为:待测溶液润洗锥形瓶;偏高;
(3)根据酸式滴定管用蒸馏水洗净后,应用标准液润洗,故答案为:用标准液润洗滴定管2~3次;
(4)V(标准)═[(20.38-0.40)+(24.02-4.00)]mL÷2═20.00mL
C(待测)═$\frac{c(标准)×V(标准)}{V(待测)}$═$\frac{0.1000mol•L×20.00mL}{25.00mL}$═0.0800mol•L-1,
故答案为:0.0800.
点评 本题主要考查了中和滴定操作以及注意事项,难度不大,应注意相关知识的积累.


科目:高中化学 来源: 题型:实验题
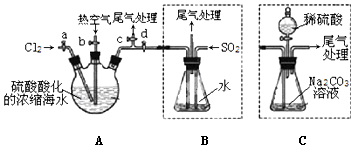
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
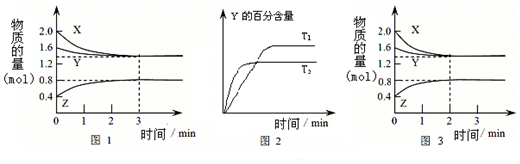
| A. | 容器中发生的反应可表示为:2X(g)+Y(g)?2Z(g) | |
| B. | 0~3 min内,v(X)=0.2 mol•L-1•min-1 | |
| C. | 其他条件不变升高温度,v正、v逆都增大,且重新平衡前v正>v逆 | |
| D. | 若改变条件,使反应进程如图3所示,则改变的条件可能是增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
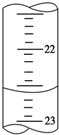 某课外活动小组欲用0.10mol/L的NaOH溶液滴定0.10mol/L的稀盐酸,其操作步骤如下:
某课外活动小组欲用0.10mol/L的NaOH溶液滴定0.10mol/L的稀盐酸,其操作步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.60 | 20.50 |
| 第二次 | 10.00 | 3.00 | 23.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
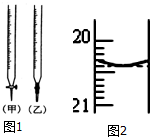 某校化学兴趣小组采用酸碱中和滴定法用0.1000mol/LNaOH溶液滴定待测盐酸溶液,试回答下面的问题:
某校化学兴趣小组采用酸碱中和滴定法用0.1000mol/LNaOH溶液滴定待测盐酸溶液,试回答下面的问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
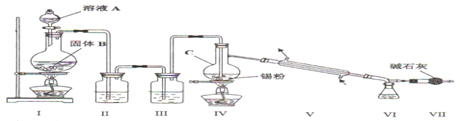
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com