
 +NaOH→
+NaOH→ +H2O.
+H2O. ;
; .
.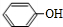 +
+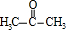 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$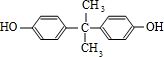 +H2O由D生成N的反应类型是缩聚反应
+H2O由D生成N的反应类型是缩聚反应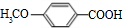 .
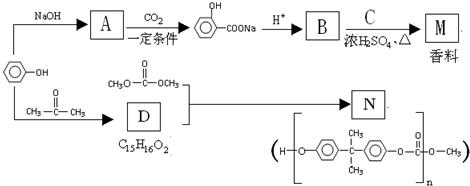
. 分析 苯酚与氢氧化钠反应生成苯酚钠,故A为 ,由转化关系可知B为
,由转化关系可知B为 ,C的分子式为C5H12O,C能与金属Na反应,属于饱和一元醇,C的一氯代物有2种,分子中有2种H原子,故C的结构简式是
,C的分子式为C5H12O,C能与金属Na反应,属于饱和一元醇,C的一氯代物有2种,分子中有2种H原子,故C的结构简式是 ,B与C发生酯化反应生成M,则M为
,B与C发生酯化反应生成M,则M为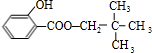 .苯酚与丙酮反应生成D,D的分子式为C15H16O2,再结合N的结构可知D为
.苯酚与丙酮反应生成D,D的分子式为C15H16O2,再结合N的结构可知D为 ,据此解答.
,据此解答.
解答 解:苯酚与氢氧化钠反应生成苯酚钠,故A为 ,由转化关系可知B为
,由转化关系可知B为 ,C的分子式为C5H12O,C能与金属Na反应,属于饱和一元醇,C的一氯代物有2种,分子中有2种H原子,故C的结构简式是
,C的分子式为C5H12O,C能与金属Na反应,属于饱和一元醇,C的一氯代物有2种,分子中有2种H原子,故C的结构简式是 ,B与C发生酯化反应生成M,则M为
,B与C发生酯化反应生成M,则M为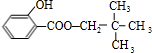 .苯酚与丙酮反应生成D,D的分子式为C15H16O2,再结合N的结构可知D为
.苯酚与丙酮反应生成D,D的分子式为C15H16O2,再结合N的结构可知D为 .
.
(1)苯酚与氢氧化钠反应生成苯酚钠,反应方程式为: +NaOH→
+NaOH→ +H2O,
+H2O,
故答案为: +NaOH→
+NaOH→ +H2O;
+H2O;
(2)C的结构简式是 ,与C含有相同官能团的同分异构,可以看作戊烷被羟基取代,正戊烷被羟基取代有3种,异戊烷被羟基取代有4种,新戊烷被羟基取代得到C,不含C共有7种,
,与C含有相同官能团的同分异构,可以看作戊烷被羟基取代,正戊烷被羟基取代有3种,异戊烷被羟基取代有4种,新戊烷被羟基取代得到C,不含C共有7种,
故答案为:7; ;
;
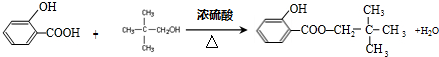
(3)B与C反应的化学方程式是: ,
,
故答案为: ;
;
(4)由苯酚生成D的化学方程式是:2 +
+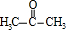 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +H2O;生成N的反应类型是缩聚反应
+H2O;生成N的反应类型是缩聚反应
故答案为:2 +
+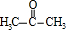 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +H2O;缩聚反应;
+H2O;缩聚反应;
(5)以苯酚为基础原料也可以合成防腐剂F.经质谱分析F的相对分子质量为152,其中氧元素的质量分数为31%,则分子中氧原子数目为$\frac{152×31%}{16}$=3,芳香族化合物F能与NaHCO3溶液反应,且不能发生水解反应,故分子中含有苯环、-COOH,假定为二元取代,则剩余基团的相对分子质量为152-76-45=31,且含有1个O原子,完全燃烧只生成CO2和H2O,故剩余基团为-OCH3或-CH2OH,故F的分子式为C8H8O3,F的核磁共振氢谱显示其分子中含有4种氢原子,分子结构中不存在“-O-O-”的连接方式,F的结构简式是 ,
,
故答案为:C8H8O3, .
.
点评 丙酮考查有机物的推断,涉及酚、羧酸等性质与转化,注意根据苯酚、D的分子式、N的结构式推断D的结构,注意(5)中利用相对分子质量确定F的分子式,是对有机化合物知识的综合考查,能较好的考查学生思维能力,是高考热点题型,难度中等.


科目:高中化学 来源: 题型:解答题
 ③白磷 ④氯气
③白磷 ④氯气 ⑥${\;}_{17}^{37}$Cl ⑦${\;}_{17}^{35}$Cl ⑧红磷
⑥${\;}_{17}^{37}$Cl ⑦${\;}_{17}^{35}$Cl ⑧红磷 ,含四原子核10电子的阳离子离子符号H3O+,含四原子核18电子的共价化合物化学式H2O2.
,含四原子核10电子的阳离子离子符号H3O+,含四原子核18电子的共价化合物化学式H2O2.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | N2O结构式可表示为N=N=O | |
| B. | O3分子呈直线形 | |
| C. | CH2=CH-CHO分子中碳原子均采用sp2杂化 | |
| D. | 相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
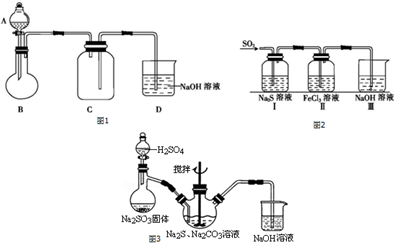
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe3+是人体所需微量元素 | B. | 苯酚不能用于杀菌消毒 | ||
| C. | 氢气是未来的一种理想燃料 | D. | 乙醇是不可再生的生物质能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过“扫描隧道显微镜”操纵原子“书写”文字 | |
| B. | 14C考古断代 | |
| C. | 煤焦油分馏得到苯及其同系物 | |
| D. | 粮食酿酒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质(少量杂质) | 操作 | |
| A | KNO3固体(NaCl) | 加水溶解、蒸发结晶、趁热过滤、洗涤、干燥 |
| B | NaCl固体(KNO3) | 加水溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| C | FeCl3溶液(NH4Cl) | 加热蒸干、灼烧 |
| D | NH4Cl溶液(FeCl3) | 滴加氨水至不再产生沉淀为止,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
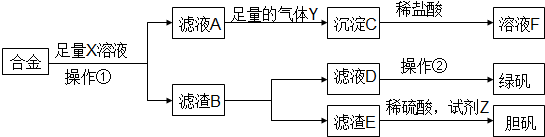
| A. | 溶液X为稀硫酸,气体Y为氨气 | |
| B. | 由溶液F获得溶质F固体的过程中,须控制条件防止其氧化和分解 | |
| C. | 使用足量稀硫酸时,试剂Z选用H2O2或适量HNO3均获得胆矾晶体 | |
| D. | 操作①为过滤,操作②为蒸发结晶、洗涤、干燥 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com