
【题目】某同学在常温下设计以下实验流程探究Na2S2O3的化学性质。下列说法正确的是

A. 实验①说明Na2S2O3溶液中水电离的c(OH-)=10-8mol·L-1
B. Na2S2O3溶液pH=8的原因用离子方程式表示为S2O32-+2H2O![]() H2S2O3+2OH-
H2S2O3+2OH-
C. 生成的沉淀B可能是BaSO3或BaSO4,要进一步确认还需加入稀硝酸验证
D. 实验②说明Na2S2O3具有还原性
【答案】D
【解析】
根据盐类的水解的规律和氧化还原反应的规律进行分析解答。
A.Na2S2O3的溶液pH=8,说明S2O32-水解,水的电离受到了促进,由水电离的c(OH-)![]() 10-6 mol·L-1,故A错误;
10-6 mol·L-1,故A错误;
B.S2O32-水解是分步进行的,S2O32-+H2O![]() HS2O3-+OH-,故B错误;
HS2O3-+OH-,故B错误;
C.两个错误点(1)氯水足量,沉淀中不可能有BaSO3(2)BaSO3与硝酸发生氧化还原反应生成BaSO4,不能加硝酸验证,故C错误;
D.S2O32-+5H2O+4Cl2+2Ba2+=2BaSO4↓+8Cl-+10H+ ,S元素的化合价升高,说明Na2S2O3具有还原性,故D选项正确;
正确答案:D。


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】金属铟主要用于生产液晶显示器和平板屏幕。从LCD废料(主要成分是含铟、锡的氧化物)中回收铟的工艺流程如下:
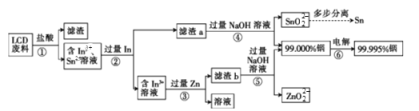
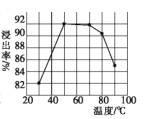
(1)步骤①中用盐酸酸浸时浸出率随温度变化关系如图所示,则最适宜的温度是___________,温度升高浸出率下降的原因是__________
(2)酸浸时铟的氧化物转化成In3+的离子方程式是__________
(3)提纯粗铟的方法和铜的精炼原理相似,则粗铟为__________(填“阴极”或“阳极”),写出阴极的电极反应式: ______________________________
(4)步骤④中所发生氧化还原反应的氧化剂是__________(填化学式),步骤⑤中所发生氧化还原反应的氧化产物与还原产物系数之比是__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟化锂(LiF)难溶于水,可用于核工业、光学玻璃制造等。以透锂长石(含Li2O、Al2O3、SiO2)为原料制备氟化锂的工艺流程如下:
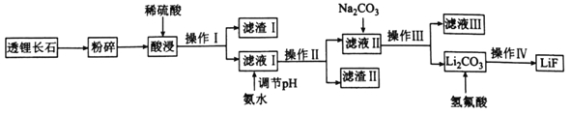
回答下列问题:
(1)滤液I中含有的金属离子有________,滤渣I的一种用途是________________。
(2)滤渣Ⅱ是目前应用最广泛的无机阻燃剂,写出生成滤渣Ⅱ的离子方程式:________________。常温下,若向滤液I中滴加氨水调节pH=5时,溶液中c(Al3+)=________mol·L-1,则溶液中A13+________(填“是”或“否”)沉淀完全(已知Ksp[Al(OH)3]=2.0×10-33,且溶液中的离子浓度小于1.0×10-5mol·L-1时沉淀完全)。
(3)操作Ⅳ包括________________、________________和干燥。
(4)写出Li2CO3与氢氟酸反应的化学方程式:________________________,该反应不能在玻璃容器中进行的原因是________________________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石棉是过去常用的保温、绝热、防火材料,但现已确认为致癌物质,并正在开发它的代用品。石棉的组成可用化学式CaMg3(SiO3)4。表示,其中Si的化合价是 ( )
A. +2 B. -2 C. +4 D. -4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是( )

A. 放电时,负极的电极反应为:H2-2e-=2H+
B. 充电时,阳极的电极反应为:Ni(OH)2+OH--e-=NiO(OH)+H2O
C. 充电时,将电池的碳电极与外电源的正极相连
D. 放电时,OH-向镍电极作定向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硅孔雀石[主要成分为CuCO3·Cu(OH)2、CuSiO3·2H2O,含SiO2、FeCO3、Fe2O3等杂质]为原料制备CuCl2的工艺流程如下:

已知: SOCl2+H2O![]() SO2↑+2HCl↑,下列说法不正确的是
SO2↑+2HCl↑,下列说法不正确的是
A. “酸浸” 时应该用盐酸溶解硅孔雀石粉
B. “氧化”时发生反应的离子方程式为:Cl2+2Fe2+![]() 2Fe3++2Cl-
2Fe3++2Cl-
C. “调pH”时,pH需控制在碱性区域,保证铁元素全部以Fe(OH)3形式除去
D. “加热脱水”时,加入SOCl2的目的是生成的HCl抑制CuCl2的水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应中,反应混合物A、B、C的物质的量浓度(c)与时间(t)关系如下所表示

下列说法错误的是( )
A. 该反应的化学方程式为2A![]() 4B+C B. 逆反应是放热反应
4B+C B. 逆反应是放热反应
C. 4min时A的转化率约为31% D. 4~6min时,反应处于动态平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)![]() 3C(g)+4D(g)反应中,表示该反应的反应速率最快的是
3C(g)+4D(g)反应中,表示该反应的反应速率最快的是
A. v(A)=0.5 mol/(L·min) B. v(B)=0.1 mol/(L·s)
C. v(C)=0.8 mol/(L·min) D. v(D)=1 mol/(L·min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com