
��14�֣��ס��ҡ����dz������������ʣ�����֮������ͼ��ʾ��ת����ϵ������Ҫ��ش����⣺
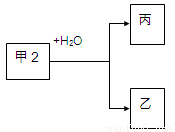
I����֪�����dz������ʣ���Ϊ������
��1������Ϊ���������д��ԣ����ҷ������ȷ�Ӧ�Ļ�ѧ����ʽΪ ��
��2������Ϊ̼��������ҡ����ɺϳɼ״���
����֪��CH4(g)��H2O(g) CO(g)��3H2(g) ��H����206.0 kJ��mol��1
CO(g)��3H2(g) ��H����206.0 kJ��mol��1
CH4(g)��H2O(g) CH3OH(g)��H2(g) ��H����77.0 kJ��mol��1
CH3OH(g)��H2(g) ��H����77.0 kJ��mol��1
д�����������������Ӧ����CH3OH(g)���Ȼ�ѧ����ʽ��__________________��
���Һͱ��ϳɼ״��ķ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)���±�����T1 ______ T2���>������<������=������
�¶�/�� | T1 | T2 |
K | 2.041 | 0.012 |
���ҿ���ij����ȼ�ϵ�ص�ȼ�ϣ��õ�صĸ�����ӦʽΪ_________________��
II����֪�����������ֶ�����Ԫ����ɵĻ��������ˮ��Һ�Լ��ԡ�
��3�������ɼ����������Ӹ�����Ϊ2:3���������塣�ɼ����������Ӱ뾶��С��ϵΪ ���þ��������ʾ����
��4��������O2�����һ����Ҫ��;�� ���������Cl2��2:1�����ʵ�������Ӧ�õ�����Һ������Һ��������Ũ�ȴӴ�С��˳���� ��
��1��3Fe3O4+8Al= 9Fe+4Al2O3
9Fe+4Al2O3
��2����CO(g)+2H2(g)=CH3OH ��H=-129 kJ��mol-1,
�� < ��CO-2e��+4OH��=CO32- +2H2O
��3��N>Mg
(4)��������Ư�� C(Cl��)>C(ClO��)>C(OH��)
��������
�����������1��Fe3O4 �׳ƴ�������������Ϊ���������д��ԣ�˵������Fe3O4 ��Fe3O4 �������ȷ�Ӧ�Ļ�ѧ����ʽΪ��3Fe3O4+8Al= 9Fe+4Al2O3 ��
9Fe+4Al2O3 ��
��2���ټ�Ϊ̼��̼��ˮ������Ӧ����CO��H2��CO��H2�ɺϳɼ״�����ѧ��ӦΪCO+2H2 =CH3OH ,���ݸ�˹���ɣ���ʽ��һʽ��77.0-206.0=-129kJ��mol-1,��CO���������ɼ״����Ȼ�ѧ����ʽΪ��CO(g)+2H2(g)=CH3OH ��H=-129 kJ��mol-1,
��CO�������ϳɼ״��ķ�Ӧ�Ƿ��ȷ�Ӧ�������¶����ߣ�Kֵ��С��T1<T2��
����ΪCO��CO������ȼ�ϵ�ص�ȼ�ϣ�COʧ��������CO2 ���ڼ��Ի����У�CO2 ��Ӧ����̼���Σ���õ�صĸ�����ӦΪ��CO-2e��+4OH��=CO32- +2H2O��
��3����Ϊ�����ұ���ˮ��Һ�Լ��ԣ���ΪNH3 �����������ֶ�����Ԫ����ɵĻ������ҹ��ɼ����������Ӹ�����Ϊ2:3�������Mg3N2 ������þ��ˮ��Ӧ���ɰ�����������þ�����ɼ����������Ӱ뾶��С��ϵΪN>Mg��
��4��������O2������ˮ��Һ�Լ��ԣ����������ֶ�����Ԫ����ɵĻ�������ΪNa2O2 ������������ˮ��Ӧ����������NaOH���������Ƶ�һ����Ҫ��;����Ư������ΪNaOH��NaOH������2:1��Ӧ�Ļ�ѧ����ʽΪCl2+2NaOH=NaCl+NaCl0+H2O��ClO�������������ӣ���ˮ�⣬���±�Cl�����٣�����Һ��������Ũ�ȴӴ�С��˳����C(Cl��)>C(ClO��)>C(OH��)��
���㣺���鳣��������ƶϼ����ʡ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�����и���һģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A����ԭ��Ⱦ�ϵ����Ľṹ��ʽΪ��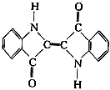 �����ķ���ʽ�ǣ�C16H10N2O2
�����ķ���ʽ�ǣ�C16H10N2O2
B���ṹΪ����CH��CH��CH��CH��CH��CH��CH��CH�����ĸ߷��ӻ�����䵥������ϩ
C��������һ��ʱ����Ȳ����ȩ���۰�ʲô������ϣ���ȫȼ������������������CO2������
D����ϩ�ᣨCH2=CHCOOH����ɽ���ᣨCH3CH=CHCH=CHCOOH������ͬϵ�������������ַ�Ӧ��IJ���Ҳ����ͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и�����ѧ����Ͽ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ������������ɳ�����չ������ء������й������в���ȷ����
A������ˮ���������Խ������ˮ��ӦΣ������������������ʹ��ˮ����
B�����ü��ȷ���������Ŀ����ʹ�����ʱ��Զ�ɱ��ϸ��
C�������ؽ����ĵ�����Ʒ�������ⶪ����Ҫ������ղ�����
D��ú̿ȼ�չ����а�װ������װ�ã���Ҫ��Ϊ�˼��ٶ���������ŷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡȪ���и���3�½�ѧ����������ۻ�ѧ�Ծ��������棩 ���ͣ������
��14�֣�
I���ס��ҡ��������������ʴ���ת����ϵ��
��1�����ס��Ҿ�Ϊ������Ҫ�ɷ֣�������Ԫ�صļ������ӵĽṹʾ��ͼΪ ��
��2��������������������ʣ������������ӷ���ʽΪ ��
��3������������ǿ��������ǿ�Ӧ������Ļ�ѧʽΪ ����д1�֣���
II��һ���¶��£��ݻ�Ϊ1 L���ܱ�������Ͷ��0.5 mol PCl5(g)������ƽ�⣺PCl5(g) PCl3(g)+ Cl2(g)����Ӧ�����в�ò����������±���
PCl3(g)+ Cl2(g)����Ӧ�����в�ò����������±���
ʱ�� | n(PCl5)/mol | n(PCl3)/mol | n(Cl2)/mol |
0 | 0.5 | 0 | 0 |
t1 | 0.45 | ||
t2 | 0.1 | ||
t3 | 0.4 |
��4��t1ʱ�̣���÷�Ӧ���յ�����Ϊa kJ��PCl3(g)��Cl2(g)��Ӧ���Ȼ�ѧ��Ӧ����ʽΪ ��
��5��t2ʱ��v�� v�棨�>������<����=������
��6����ͬ�¶��£���Ϊ��������Ͷ��0.2 mol PCl5(g)��0.2 mol PCl3(g)��0.1 mol Cl2(g)������ƽ
��ǰ��PCl5�����ʵ����� �����������С���������䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡȪ���и���3�½�ѧ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������Ӻ�ˮ�л�õ���
A������ B���Ȼ�þ C���� D����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�����ѧ����������ۻ�ѧ�Ծ� �������棩 ���ͣ�ѡ����
��KIΪ����ļӵ�ʳ�Σ������ܿ������ã�������������ʧ����ҵ�������������ȶ����Լ��ٵ����ʧ�����������п������ȶ�������
A��Na2S2O3 B��FeCl3 C��NaHCO3 D��CaO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ��������ɽ����ѧ�ڸ�һ��ѧ��ĩ�Ծ��������棩 ���ͣ�ѡ����
�ں�1mol KAl(SO4)2����Һ����μ��뺬2mol Ba(OH)2����Һ������˵������ȷ����
A�������ɳ����������ȫ���ܽ�
B������Һ��Al3+ȫ����������ʱ�������������ʵ������
C�����õ��ij�����BaSO4
D�����ij���Ϊ2mol BaSO4��1mol Al(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ��ͷ�е���У�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ������
��12�֣�����ͭ���ʼ��仯����Ӧ�÷�Χ�ܹ㡣���к��Ȼ��������ʵ��Ȼ�ͭ����(CuCl2��2H2O)�� Ϊ��ȡ������CuCl2��2H2O�����Ƚ����Ƴ�ˮ��Һ��Ȼ����ͼ��������ᴿ��

��֪Cu2+��Fe3+��Fe2+���������↑ʼ�����ͳ�����ȫʱ��pH�����±���
Fe3+ | Fe2+ | Cu2+ | |
�������↑ʼ����ʱ��pH | 1.9 | 7.0 | 4.7 |
����������ȫ����ʱ��pH | 3.2 | 9.0 | 6.7 |
��ش��������⣺
��1���õ���ҺII�������������X, ���ʺ���������X���� ��
A��K2Cr2O7 B��NaClO C��H2O2 D��KMnO4
��2������������X��Ŀ���� ��
��3��Ϊ�˳�ȥFe3+�����������Y������Һ��PHֵΪ
��4������ܲ���ֱ�������ᾧ�õ�CuCl2��2H2O����? (��ܡ����ܡ�)�����ܣ����ûش������ܣ��ش����β���? ��
��5����֪Fe(OH)3��Ksp=1��10-35mol4/L4 ����Fe3+������ȫʱ������Һ��Fe3+��Ũ��Ϊ1��10-5mol/L�� ���ʱ��Һ��PH��СΪ .
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����
A��������ˮ��pHΪ7.0�������pHС��7.0
B���ϸ�ִ�л�����β���ŷű������ڷ�ֹ������Ⱦ
C��ʹ�ö��������ijЩ������Ư��ʳƷ������彡������Σ��
D��ʹ������������ˮ���������У����ɵ��л��Ȼ�����ܶ������к�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com