
分析 (1)N4气体转变为N2气体先破坏N4分子N-N键吸收能量,再生成N2分子形成N≡N键放出能量,注意一个N4分子中含有6个N-N键,根据能量的变化写出热化学反应方程式;
(2)原电池中,负极上失去电子发生氧化反应,注意结合电解质溶液的酸碱性写电极反应式;
(3)根据三段式计算出各组分的物质的量的变化量、平衡时各组分的物质的量;
①平衡常数指生成物浓度的系数次幂之积与反应物浓度系数次幂之积的比值,即K=$\frac{c({O}_{2}){c}^{4}(N{O}_{2})}{{c}^{3}({N}_{2}{O}_{5})}$;
②根据v=$\frac{△c}{△t}$计算v(O2);
③该反应为吸热反应,降低温度平衡向逆反应进行,再根据选项具体分析;
(4)平衡后分别再充入NO2和再充入N2O4,相当于增大体系压强,二氧化氮平衡转化率增大,平衡时N2O4与NO2的物质的量之比为a增大;
(5)根据氨水电离生成等量的铵根离子和氢氧根离子,由电离平衡常数求出平衡时氢氧根离子的浓度;25℃时时,Mg(OH)2的溶度积常数Ksp=1.8×10-11,pH=11.0,c(OH-)=0.001mol/L,以此计算.
解答 解:(1)根据原子守恒知,一个N4分子生成2个N2分子,一个N4分子中含有6个N-N键,破坏1molN4分子中含有6molN-N键需要吸收167kJ/mol×6mol=1002kJ能量;
生成2molN≡N键放出942kJ/mol×2mol=1884kJ能量,所以该反应放出1884kJ-1002kJ=882kJ能量,所以热化学反应方程式为N4(g)=2N2(g)△H=-882kJ/mol,
故答案为:N4(g)=2N2(g)△H=-882kJ/mol;
(2)原电池中,负极上失去电子发生氧化反应,该反应中氨气发生氧化反应,所以负极上发生的反应是:氨气失电子和氢氧根离子反应生成氮气和水,电极反应式为
2NH3+6OH--6e-=N2+6H2O,故答案为:2NH3+6OH--6e-=N2+6H2O;
(3)令平衡时O2的物质的量为nmol,则
对于反应 2N2O5(g)?4NO2(g)+O2(g),
开始(mol):5 0 0
变化(mol):2n 4n n
平衡(mol):5-2n 4n n
所以 $\frac{4n}{(5-2n)+4n+n}$×100%=50%,解得n=1,
①由上述计算知平衡时N2O53mol、NO24mol、O21mol.所以平衡时N2O5的浓度为 $\frac{3mol}{10L}$=0.3mol/L,平衡时NO2的浓度为 $\frac{4mol}{10L}$=0.4mol/L,平衡时O2的浓度为$\frac{1mol}{10L}$=0.1mol/L,
所以平衡常数k=$\frac{c({O}_{2}){c}^{4}(N{O}_{2})}{{c}^{3}({N}_{2}{O}_{5})}$=$\frac{0.1×0.{4}^{4}}{0.{3}^{3}}$,
故答案为:$\frac{0.1×0.{4}^{4}}{0.{3}^{3}}$;
②由上述计算知平衡时O2的质的量为1mol,
从0~5min内用O2表示该反应的平均速率v(O2)=$\frac{\frac{1mol}{10L}}{5min}$=0.02mol/(L•min),
故答案为:0.02mol/(L•min);
③A.该反应正反应为吸热反应,降低温度平衡向逆反应进行,由于反应前气体体积比反应后小,所以压强减小,故A正确;
B.都为气体,总质量不变,体积不变,所以密度不变,故B错误;
C.温度降低,反应速率降低,故C正确;
D.该反应正反应为吸热反应,降低温度平衡向逆反应进行,N2O5的浓度增加,故D错误.
故选:AC;
(4)在恒温恒容的密闭容器中充入NO2,建立如下平衡:2NO2(g)?N2O4(g),平衡后分别再充入NO2和再充入N2O4,相当于增大体系压强,二氧化氮平衡转化率增大,平衡时N2O4与NO2的物质的量之比为a增大;
故答案为:B.
(5)已知氨水电离生成等量的铵根离子和氢氧根离子,NH3•H2O的电离平衡常数为Kb=$\frac{c(N{{H}_{4}}^{+})c({H}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{{c}^{2}(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{{c}^{2}(O{H}^{-})}{0.5mol/L}$=1.8×10-5 ,所以c(OH-)=3×10-3mol/L,则c(H+)=$\frac{1}{3}$×10-11mol/L,所以PH=11.5;
①25℃时时,Mg(OH)2的溶度积常数Ksp=1.8×10-11,pH=11.0,c(OH-)=0.001mol/L,残留在溶液中的c(Mg2+)=$\frac{Ksp}{{c}^{2}(O{H}^{-})}$=$\frac{1.8×1{0}^{-11}}{(0.001)^{2}}$=1.8×10-5mol/L,
故答案为:11.5;1.8×10-5mol/L;
点评 本题考查了反应热、原电池电极反应、平衡常数反应速率的影响因素分析判断,化学平衡移动、化学平衡常数及计算等,难度中等,考查学生分析和解决问题的能力和对知识的掌握.


 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 水的电离平衡曲线如图所示,若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是( )
水的电离平衡曲线如图所示,若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是( )| A. | 改变条件使纯水的pH值减小,其酸性增强 | |
| B. | 100℃时某溶液中由水电离产生的c(H+)=1×10-11 mol•L-1,则该溶液的pH可能是11或3 | |
| C. | 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10:1 | |
| D. | 100℃时,pH值均为8的醋酸钠和氨水两溶液中,水的电离程度之比为104:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
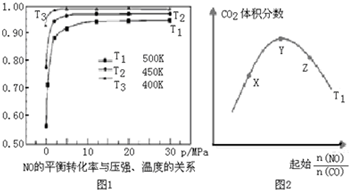
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
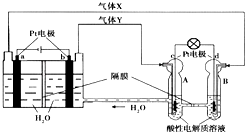 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )| A. | 当有0.1mol电子转移时,a极产生1.12L O2(标况) | |
| B. | b极上发生的电极反应是:2H++2e-═H2↑ | |
| C. | d极上发生的电极反应是:O2+4H++4e-═2H2O | |
| D. | c极上进行还原反应,B中的H+可以通过隔膜进入A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
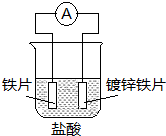
| A. | 溶液中pH值明显下降 | B. | 阴极的电极反应式:Fe-2e→Fe2+ | ||
| C. | 铁片为正极,镀锌铁片为负极 | D. | 电子由锌经溶液流向铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯碱工业是电解熔融的NaCl,阳极产生Cl2 | |
| B. | 氢氧燃料电池可将热能直接转化为电能 | |
| C. | 原电池工作时,电子从负极经外电路移向正极 | |
| D. | 工业上电解熔融的AlCl3来制取铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com