
【题目】菠菜具有丰富的营养。民间流传:菠菜与豆腐不宜同时食用。
资料:(1)菠菜中含有可溶性草酸盐、碳酸盐等
(2)醋酸不与草酸钙反应
(3)某草酸钙晶体(CaC2O4·xH2O)的相对分子质量为128+18x
【实验一】菠菜中部分成分分析

(1)用开水煮沸菠菜样品碎末2~3 min的目的是___________________。
(2)溶液M中含有的主要阴离子有____________________。
(3)已知C能使澄清石灰水变浑浊。A与醋酸生成C的化学方程式是__________。
(4)B的化学式可能是________________。
(5)草酸比碳酸的酸性___________(填“强”或“弱”)。
【实验二】对某草酸钙晶体进行热分解研究,得到相关数据如图所示。

(1)800℃时得到的固体只含钙元素和氧元素,质量比为5:2,其化学式是__________。
(2)固体质量由12.8 g变为10.0 g的过程中发生反应的化学方程式是__________。
(3)x =_____________。
【答案】 充分浸出可溶物 C2O42-、CO32- 2CH3COOH + CaCO3 === (CH3COO)2Ca + CO2↑ + H2O CaC2O4 强 CaO CaC2O4![]() CaCO3 + CO2↑ 1
CaCO3 + CO2↑ 1
【解析】实验一:(1)用开水煮沸菠菜样品碎末有利于使样品中的可溶物充分溶解,故答案为:充分浸出可溶物。(2)由资料:菠菜中含有可溶性草酸盐、碳酸盐等,溶液M中含有的主要阴离子有C2O42-、CO32-。(3)因气体C能使澄清石灰水变浑浊,则C为二氧化碳,根据信息醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐,则加醋酸时碳酸钙和醋酸反应生成了二氧化碳,沉淀A为草酸钙和碳酸钙的混合物,沉淀B为草酸钙,故答案为:CaCO3+2 CH3COOH=(CH3COO)2Ca +H2O+CO2↑;(4)由上分析知,沉淀B为草酸钙,化学式为:CaC2O4。(5)根据强酸制弱酸原理,醋酸酸性大于碳酸酸性,又因为醋酸不能溶解草酸钙,所以草酸酸性大于醋酸酸性,故草酸比碳酸的酸性强。
实验二:(1)根据图象可知600℃时发生碳酸钙分解反应,800℃时得到的固体只含钙元素和氧元素,质量比为5:2,则N(Ca):N(O)=1:1,固体成分为CaO。(2)400℃时草酸钙分解,其质量由12.8g变为10.0g,生成碳酸钙和CO气体,方程式是:CaC2O4 ![]() CaCO3 + CO ↑。(3)根据图象可知0~200℃是晶体失去结晶水的过程,14.6克CaC2O4xH2O失去水后生成12.8克CaC2O4,根据
CaCO3 + CO ↑。(3)根据图象可知0~200℃是晶体失去结晶水的过程,14.6克CaC2O4xH2O失去水后生成12.8克CaC2O4,根据
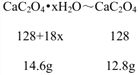 ,
,
所以x=1。


科目:高中化学 来源: 题型:
【题目】海洋中蕴含着丰富的资源。利用海水提取淡水、溴和镁的部分过程如图所示。

(1)海水淡化的方法有___________、离子交换法和电渗析法等。
(2)用纯碱吸收浓缩海水吹出的Br2:3Br2+ 6Na2CO3+3H2O=5NaBr+NaBrO3+6NaHCO3。若吸收3 mol Br2时,转移的电子是________ mol。
(3)海水中部分离子的含量如下:
成分 | 含量(mg/L) | 成分 | 含量(mg/L) |
Na+ | 10560 | Cl- | 18980 |
Mg2+ | 1272 | Br- | 64 |
Ca2+ | 400 | SO42- | 2560 |
其中,Mg2+的物质的量浓度是_____________ mol/L。若从100 L的海水中提取镁,理论上加入沉淀剂Ca(OH)2的质量是____________ g。
(4)由Mg(OH)2得到单质Mg,以下方法最合适的是__________(填序号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅广泛应用于计算机技术领域。工业上,用焦炭在电炉中还原二氧化硅制得粗硅。某研究性学习小组在实验条件下对过量炭粉与二氧化硅反应的气体产物成分进行探究。
(1)提出假设
①该反应的气体产物是CO2
②改反应的气体产物是CO
③该反应的气体产物是_________。
(2)设计方案,利用如图所示装置进行实验

(3)查阅资料
①在该实验条件下氮气不与碳、硅、二氧化硅发生反应
②实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热制得氮气

氮气的发生装置可以选择上图中的____,反应的化学方程式为_________。
(4)实验步骤
①连接好装置后,称取12.0g二氧化硅,10.0g碳粉混合均匀,放入质量为48.0g的硬质玻璃管中。放入药品前应进行的操作是__________
②打开弹簧夹,向装置中通入纯净干燥的氮气。
③停止通入氮气后,夹紧弹簧夹,加热一段时间,发现澄清石灰水(足量)变浑浊。
④待反应结束,停止加热,再缓缓通入一段时间的氮气,冷却至室温,称得硬质玻璃管和固体总质量为60.0g。再缓缓通入氮气的作用为_____________
⑤将石灰水过滤、洗涤、烘干,称量固体质量为10.0g。该操作中过滤、洗涤时用到的玻璃仪器是_____;至少称量____次。
(5)数据处理
根据所得实验数据,该实验中二氧化硅与碳发生反应的化学方程式为_________
(6)实验优化
学习小组有同学认为对实验装置需要进一步完善、改进:
①_______________;②将澄清石灰水换成浓氢氧化钡溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生活中有着广泛的应用,下列对立关系正确的是( )
选项 | 化学性质 | 实际应用 |
A | SO2具有还原性 | 漂白纸浆 |
B | HF具有弱酸性 | 在玻璃上刻字, |
C | 铝的金属活动性强于氢 | 用铝制容器贮运浓硝酸 |
D | FeCl3溶液能与Cu反应 | 蚀刻铜箔制造电路板 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+H2O(g)=CO(g)+H2(g) △H=a kJ/mol
C(s)+O2(g)=2CO(g) △H=-220 kJ/mol
H-H、O=O和O-H键的键能分别为436、496和462 kJ/mol,则a为( )
A.-332
B.-118
C.+350
D.+130
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组利用以下装置进行电解氯化铵溶液的实验,其中X为铁,Y为石墨,a为wg质量分数为40%的NH4Cl溶液(滴有酚酞)。
已知:①氧化性:Cl2> Br2>O2 > I2,②NH3+3CuO![]() 3Cu + 3H2O + N2
3Cu + 3H2O + N2

(l)电解过程中,A 装置中可观察到的现象是__________。
(2)请选用上述仪器,组装一套检验产生氢气的装置:_________[按气流方向(用“→”表示),用小写字母表示,装置不重复使用]。
(3)某同学认为将E换成装有碱石灰的干燥管也可以达到相同效果,乙同学认为不合理,其理由是________________。
(4)设计实验检测阳极产生的气体成分(除水蒸气外)。(所选的试剂用字母编号代替)限选试剂:A、3mol/LNaOH溶液 B、品红 C、酸化的淀粉-KI溶液 D、KBr溶液
操作 | 现象和结论 |
将混合气体依次通入________ | __________________ |
(5)电解结束后,加热电解液将NH3完全蒸出,并用水吸收形成200.00mL溶液,取出其中的20.00mL加指示剂后用标准浓度为c mol/L的盐酸溶液滴定,消耗盐酸V mL,则电解制得NH3的产率_________(用化简为整数的含w 、c 、V的代数式表示)。
(6)若实验时反接了正负极,则X极的电极方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 含金属元素的离子一定都是阳离子
B. 酸性氧化物都可以与NaOH溶液反应
C. 金属氧化物都是碱性氧化物
D. 合金一定是由两种或两种以上的金属融合而成的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Al(OH)3的性质叙述错误的是( )
A. Al(OH)3受热易分解生成Al2O3和H2O
B. Al(OH)3是难溶于水的白色胶状物质
C. Al(OH)3能凝聚水中的悬浮物,也能吸附色素
D. Al(OH)3既能溶于NaOH溶液、氨水,又能溶于盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com