
下列溶液中的Cl﹣浓度与50mL 1mol/L MgCl2溶液中的Cl﹣浓度相等的是()
A. 150 mL 1 mol/L NaCl溶液 B. 75 mL 2 mol/L CaCl2溶液
C. 150 mL 2 mol/L KCl溶液 D. 75 mL 1 mol/LAlCl3溶液
考点: 物质的量浓度.
专题: 物质的量浓度和溶解度专题.
分析: 根据同一化学式中各微粒的浓度等于物质的物质的量浓度×离子个数,与溶液的体积无关,1mol/L MgCl2溶液中的Cl﹣浓度为2mol/L.
解答: 解:50mL 1mol•L﹣1 MgCl2溶液中Cl﹣的物质的量浓度c(Cl﹣)=2c(MgCl2)=2mol/L,
A、150mL 1mol•L﹣1NaCl溶液中Cl﹣的物质的量浓度c(Cl﹣)=c(NaCl)=1mol/L,故A错误;
B、75mL 2mol•L﹣1CaCl2溶液中Cl﹣的物质的量浓度c(Cl﹣)=2c(CaCl2)=4mol/L,故B错误;
C、150mL2mol•L﹣1KCl溶液中Cl﹣的物质的量浓度c(Cl﹣)=c(KCl)=2mol/L,故C正确;
D、75mL1mol•L﹣1AlCl3溶液中Cl﹣的物质的量浓度c(Cl﹣)=3c(AlCl3)=3mol/L,故D错误;
故选C.
点评: 本题考查浓度的计算分析,溶液中离子的浓度只与物质的浓度和化学式有关,与溶液的体积无关.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
将下列物质按酸、碱、盐、氧化物分类排列,正确的是()
A. 硫酸、纯碱、生石灰、氧气 B. 醋酸、烧碱、硝酸钾、干冰
C. NaHSO4、乙醇、CaCO3、水 D. 硝酸、熟石灰、苛性钠、甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
将NaHSO4溶液和NaHCO3溶液混合,发生反应的离子方程式为()
A. H++HCO3﹣═H2O+CO2↑
B. 2HSO4﹣+CO32﹣═H2O+CO2↑+2SO42﹣
C. HSO4﹣+HCO3﹣═H2O+CO2↑+SO42﹣
D. 2H++CO32﹣═H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用氯酸钾和二氧化锰制取氧气的反应方程式为: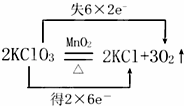 回答下列各题:
回答下列各题:
(1)该反应的基本类型为 .
(2)该反应中被还原的元素名称为 .
(3)式子“失6×2e﹣”中各数字的含义分别是 、 .
(4)从反应后的固体混合物中分离出难溶于水的MnO2操作方法:溶解、过滤、洗涤、干燥
(5)分离出的MnO2可用于实验室制取Cl2,化学方程式为MnO2+4HCl(浓) Cl2↑+MnCl2+2H2O,其离子方程式为 ,反应中浓盐酸表现的性质是(填序号)BC
Cl2↑+MnCl2+2H2O,其离子方程式为 ,反应中浓盐酸表现的性质是(填序号)BC
A 氧化性 B还原性 C酸性
(6)以上两个反应都用到MnO2,其作用分别是 、 .
(7)若两个反应中转移的电子的物质的量相同,则生成的O2和Cl2在相同状况下的体积比为.
查看答案和解析>>
科目:高中化学 来源: 题型:
除去括号内杂质所用试剂和方法不正确的是()
A. Cu(Fe)﹣﹣稀盐酸,过滤
B. KNO3(NaCl)﹣﹣结晶
C. 水(NaCl)﹣﹣蒸馏
D. CO2(HCl)﹣﹣氢氧化钠溶液,洗气
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氧化性强弱顺序:Cl2>Br2>Fe3+>I2.下列反应或叙述不正确的是()
A. Br2+2HI=I2+2HBr
B. 2FeCl2+Cl2=2FeCl3
C. 2FeCl2+2HCl+I2=2FeCl3+2HI
D. 少量Cl2通入到NaBr和NaI的混合溶液中,Cl2优先氧化I﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
现有三种可溶性物质A、B、C,其中有一种是碱、两种是盐,溶于水后电离产生的离子如表所示:
阳离子 Na+ H+ Ba2+
阴离子 OH﹣ CO32﹣ SO42﹣
为鉴别它们,分别完成一些实验.请根据实验的结果回答下列问题:
(1)A溶液与B溶液反应可生成气体X.根据上述六种离子之间的可能反应判断X的化学式为CO2,A溶液与B溶液反应的离子方程式为 .
(2)气体X可以和C溶液反应生成沉淀D,沉淀D可与B溶液反应.则C的化学式为 ,B溶液的电离方程式为 ﹣,鉴别溶液中B的阴离子的实验操作为 .
(3)B溶液与C溶液反应生成不溶于稀硝酸的白色沉淀E.B溶液与C溶液反应至中性的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
选择下列实验方法分离物质,将分离方法的序号填在横线上.
A、萃取分液法 B、加热分解C、结晶法D、分液法E、蒸馏法F、过滤法
(1) 分离饱和食盐水和沙子的混合物;
(2) 从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
(3) 用四氯化碳从碘水中提取碘;
(4) 分离四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C),已知四氯化碳和甲苯互溶.
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中所用氯气是用如下方法制取的4HCl(浓)+MnO2 Cl2↑+MnCl2+2H2O.试回答下列问题:
Cl2↑+MnCl2+2H2O.试回答下列问题:
(1)该反应是氧化还原反应吗? ,如果是氧化还原反应,请指出 是氧化剂, 是还原剂, 是氧化产物, 是还原产物.若标况下生成33.6L Cl2,则该反应中转移 mol电子.
(2)HCl在该反应中的作用为:
(3)氯气溶入水显酸性,写出该反应的离子方程式:Cl2+H2O=H++Cl﹣+HClO;氯气有毒,并有剧烈的刺激性,若吸入大量氯气,可中毒死亡,所以氯气尾气直接排入大气中,会污染环境.实验室中可采用NaOH溶液来吸收有毒的氯气,相关的离子方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com