
【题目】某学习小组利用下列装置探究氯气与氨气的反应.其中A、B分别为氯气和氨气的发生装置,C为纯净干燥的氯气与氨气反应的装置.
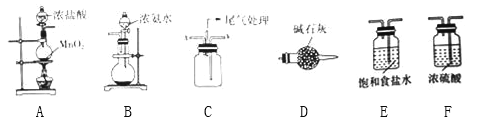
(1)若Cl2从左向右流动,NH3从右向左流动,则上述实验装置中,依次连接的合理顺序为:A→________________→B;为使NH3与Cl2更充分混合,Cl2应从C装置的__口进入(填“x”或“y”).
(2)简述装置A中使用分液漏斗向圆底烧瓶中滴加浓盐酸的操作是__________________.
(3)装置A中发生反应的离子方程式为_______________________________.
(4)装置B中圆底烧瓶内的试剂为______________(填名称).
(5)装置D的作用是____________________________.
(6)反应开始后,装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气中的主要成分之一,该反应的化学方程式为________________________________
【答案】 E、F、C、D x 打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,缓慢滴加 MnO2+4H++2C1﹣![]() Mn2++C12↑+2H2O 氢氧化钠固体、碱石灰或生石灰等 吸收水蒸气,干燥氨气 3Cl2+8NH3═N2+6NH4Cl
Mn2++C12↑+2H2O 氢氧化钠固体、碱石灰或生石灰等 吸收水蒸气,干燥氨气 3Cl2+8NH3═N2+6NH4Cl
【解析】(1)Cl2从左向右流动,NH3从右向左流动,A是氯气的发生装置,产生氯气后,用饱和食盐水吸收氯气中混有的HCl气体,再用浓硫酸干燥,制备纯净干燥的氯气;B装置是氨气的发生装置,产生氨气后,用碱石灰干燥;制得氯气和氨气在C装置中发生反应,所以上述实验装置中,依次连接的合理顺序为:A→E→F→C→D→B;由于Cl2密度比空气的密度大,为使NH3与Cl2更充分混合,Cl2应从C装置的x口进入;
(2)装置A中使用分液漏斗向圆底烧瓶中滴加浓盐酸的操作是打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,缓慢滴加;
(3)装置A中是制备氯气的发生装置,是在加热的条件下进行的反应,所用原料为二氧化锰和浓盐酸,离子方程式为:MnO2+4H++2C1﹣![]() Mn2++C12↑+2H2O;
Mn2++C12↑+2H2O;
(4)装置B是在常温下进行的反应,可以和浓氨水产生氨气的试剂可以是氢氧化钠固体、碱石灰或生石灰等,所以圆底烧瓶内的试剂为氢氧化钠固体、碱石灰或生石灰等;
(5)装置D主要用于吸收水蒸气,干燥氨气;
(6)反应开始后,装置C内出现浓厚的白烟并在容器内壁凝结,推测此物质为氯化铵固体,
另一生成物是空气中的主要成分之一,即氮气,因此该反应的化学方程式为:3Cl2+8NH3═N2+6NH4Cl。


科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: 
(1)若X极电极材料为铁,Y极电极材料为惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式是 .
②该装置的总反应方程式为
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 , Y电极的材料是 ,
②Y电极的电极反应式 . (说明:杂质发生的电极反应不必写出)
(3)若X极材料为光滑的铁钉(已经处理),Y极的材料为锌,电解质溶液a为ZnCl2 , ①X极的电极反应式为
②Y极的电极反应式为
③电解质溶液a的浓度将(填“增大”、“减少”、“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为北京奥运会的奖牌﹣﹣“金镶玉”牌,使用了昂贵的玉石材料,其化学成分多为含水钙镁硅酸盐,如Ca2Mg5Si8O22(OH)2等.下列说法正确的是( )
A.Ca2Mg5Si8O22(OH)2可用氧化物的形式表示为2CaO5MgO8SiO2H2O
B.从分类的角度看,Ca2Mg5Si8O22(OH)2为氧化物
C.玉石材料性质稳定,耐强酸和强碱的腐蚀
D.Ca2Mg5Si8O22(OH)2易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复).
阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
阴离子 | OH﹣、Cl﹣、CO |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性;
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀;
④上述沉淀包括难溶物和微溶物
(1)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: .
(2)写出E溶液与过量的B溶液反应的离子方程式 .
(3)已知:NaOH(aq)+HNO3(aq)═NaNO3(aq)+H2O(l);△H=﹣akJmol﹣1 . 请写出B与C的稀溶液反应的热化学方程式 .
(4)在100mL 0.1 molL﹣1E溶液中,逐滴加入35 mL 2 molL﹣1NaOH溶液,最终得到沉淀的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X是中学化学中的常见物质,存在如图所示转化关系(部分生成物和反应条件略去).

(1)若A为淡黄色粉末,则0.1molA与水反应时转移的电子数目为________.
(2)若A为常见的金属单质,焰色反应呈黄色;X是一种造成温室效应的气体,则鉴别等浓度的D、E两种溶液的试剂为______________.
(3)若B具有漂白性,则A与H2O反应的离子方程式:________________.
(4)若A为红棕色气体,向E溶液中滴加足量氨水,生成的白色沉淀迅速变成绿色,最终变成红褐色.
①X的化学式为__________.
②A与H2O反应的化学方程式为____________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的浓度变 化如图(Ⅰ)所示.保持其他条件不变,在T1、T2两种温度下,Y的体积分数变化如图(Ⅱ)所示.下列结论正确的是( ) 
A.t2时,保持其它条件和物质状态不变,增加压强,化学平衡向逆反应方向移动
B.T℃时,若密闭容器中各物质起始浓度为:0.4 mol/L X、0.4 mol/L Y、0.2 mol/L Z.保持其他条件不变,达到平衡时z的浓度为0.4 mol/L
C.图(Ⅱ)中T1>T2 , 则正反应是吸热反应
D.其他条件不变,升高温度,正、逆反应速率均增大,且X的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,冰醋酸加水稀释过程中溶液的导电能力有如图所示曲线,请回答. 
①a、b、c三点的氢离子浓度由小到大的顺序为 .
②a、b、c三点中,醋酸的电离程度最大的一点是 .
③测得某醋酸溶液中氢离子浓度为0.004molL﹣1 , 则醋酸的电离度为 , 该温度下醋酸的电离平衡常数K=
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com