
【题目】下列有机物中,既能跟金属钠反应放出氢气,又能发生酯化反应,还能和碳酸氢钠发生反应的是( )
A.乙酸B.乙醇C.乙酸乙酯D.水
 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
【题目】已知反应①2FeCl3+2KI![]() 2FeCl2+2KCl+I2 ②KClO3+6HCl
2FeCl2+2KCl+I2 ②KClO3+6HCl![]() KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O
③2FeCl2+Cl2![]() 2FeCl3 ,下列物质的氧化能力强弱顺序正确的是
2FeCl3 ,下列物质的氧化能力强弱顺序正确的是
A.FeCl3>Cl2>I2> KClO3 B.KClO3>Cl2> FeCl3>I2
C.Cl2>KClO3> FeCl3>I2 D.KClO3>Cl2>I2> FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于现在的元素周期表的说法中正确的是( )
A. 从左向右数第六纵行是ⅥA族
B. 所含元素形成的化合物种类最多的族是第IVA族
C. 七个周期18个族
D. ⅠA族全部是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是一种常见的滴定剂和重要化工原料。实验室制备硫代硫酸钠的流程如下:

回答下列问题:
(1)“溶解”使用的水必须先煮沸一段时间,然后冷却至室温待用。其目的是____________。
(2)“反应”中的化学方程式为_____________________________________________。
(3)设计如图所示装置制备硫代硫酸钠晶体:

①B瓶的作用是___________________。
②实验中先打开________(填“A”或“C”)处分液漏斗的活塞。.
③装置D用于处理尾气,可选用的最合理装置为______________(填标号)。

(4)为了探究粗产品中的杂质,进行如下假设并进行实验:
①该粗产品中可能含有的杂质是Na2CO3、NaHCO3、Na2SO3、NaHSO3、S、Na2S和_____________
等其中的一种或几种。
②取少量产品于试管,加入足量稀硫酸,将气体通入CuSO4溶液中,未产生黑色沉淀。据此,______(填“能”,或“不能”)认为粗产品中一定没有Na2S,理由是 _____________________________。
③请选择下列试剂设计实验方案,检验产品中含有Na2CO3或NaHCO3。
限选试剂:3 molL-1H2SO4溶液、1 mol L-1 NaOH溶液、酸性KMnO4溶液、饱和NaHCO3溶液、品红溶液、澄清石灰水。
实验方案 | _______. |
实验现象 | _______. |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是学习和研究化学的一种重要方法,下列分类合理的是
A.Na2CO3和Na2O2都属于盐 B.KOH和KHCO3都属于碱
C.H2SO4和H3PO4都属于酸 D.Na2O和Na2SiO3都属于氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示的变化,其中A为X、Y组成的双原子分子,B和C均为10电子分子。下列说法不正确的是

A.X元素位于第ⅥA族 B.A不能溶于B中
C.A和C不可能发生氧化还原反应 D.B的沸点高于C的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.20molL﹣1的H2SO4溶液中,H+的物质的量浓度为( )
A. 0.10 molL﹣1 B. 0.20 molL﹣1 C. 0.40 molL﹣1 D. 0.50 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现钼酸钠可减缓金属的腐蚀速率。工业上利用钼精矿(主要成分是不溶于水的MoS2,含少量重金属化合物)制备钼酸钠晶体( Na2MoO4·2H2O)的途径如图所示:
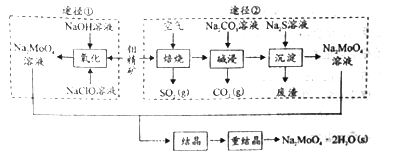
回答下列问题:
Ⅰ.(1)下列标志中,应贴在保存NaClO容器上的是____________。

(2)为了提高焙烧效率,除增大空气量外还可以采用的措施有__________________。
(3)途径①制备钼酸钠溶液,同时有SO42-生成,该反应的离子方程式为_____________。
(4)重结晶得到的母液可以在下次重结晶时重复使用,但达到一定次数后必须净化处理,原因是________________________。
(5)“结晶”前测得部分离子浓度c(MoO42-)=0.40mol/L,c(SO42-)=0.04mol/L,需加入Ba(OH)2固体除去SO42-。当BaMoO4开始沉淀时,SO42-的去除率为______%。(保留三位有效数字)。
Ⅱ.(1)碳钢在盐酸和硫酸中腐蚀速率随酸的浓度变化有明显差异,其原因可能是_____。
(2)若缓释剂钼酸钠-月桂酰肌氨酸总浓度为300mg·L-1,则缓蚀效果最好时钼酸钠的物质的量浓度为_________(保留三位有效数字)。[已知:Ksp(BaSO4)=1.1×10-10、Ksp(BaMoO4)=4.0×10-8,加入 Ba(OH)2固体引起溶液体积变化可忽略]。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017北京]2016年IUPAC命名117号元素为Ts(中文名“![]() ”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
”,tián),Ts的原子核外最外层电子数是7。下列说法不正确的是
A.Ts是第七周期第ⅦA族元素 B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱 D.中子数为176的Ts核素符号是![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com