
标准状况下a L H2和Cl2的混合气体,经光照充分反应后,所得气体恰好使溶液中b mol NaOH完全转变成盐,则a、b的关系不可能是
A.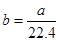 B.
B. C.
C.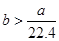 D.
D.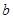 ≥
≥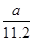
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
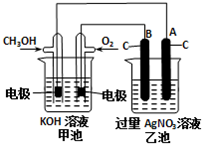 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.| 催化剂 | 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)研究NO2、SO2 、等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为 。利用反应6NO2+ 8NH3 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L 。
(2)已知:2SO2(g)+O2(g)2SO3(g) ΔH = - 196.6 kJ· mol-1
2NO(g)+O2(g)2NO2(g) ΔH = - 113.0 kJ· mol-1
则反应NO2(g)+SO2(g)SO3(g)+NO(g)的ΔH = kJ· mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K= 。
查看答案和解析>>
科目:高中化学 来源:2013届河北省高二上学期期中考试化学试卷(解析版) 题型:填空题
(10分)研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为
。利用反应6NO2+ 8NH3 7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g)
ΔH=-113.0 kJ·mol-1
2NO2(g)
ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=
kJ·mol-1。
SO3(g)+NO(g)的ΔH=
kJ·mol-1。
一定条件下,将NO2与SO2以体积比1: 2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K= 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年海南省琼海市高三第一学期教学质量监测(三)化学试卷 题型:填空题
(10分)研究NO2、SO2 、等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为
。利用反应6NO2+ 8NH3 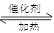 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
L 。
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
L 。
(2)已知:2SO2(g)+O2(g) 2SO3(g)
ΔH = - 196.6 kJ· mol-1
2SO3(g)
ΔH = - 196.6 kJ· mol-1
2NO(g)+O2(g) 2NO2(g)
ΔH = - 113.0 kJ· mol-1
2NO2(g)
ΔH = - 113.0 kJ· mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH =
kJ· mol-1。
SO3(g)+NO(g)的ΔH =
kJ· mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com