
某溶液可能含有Cl-、SO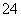 、CO
、CO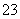 、NH
、NH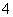 、Fe3+、Al3+和K+。取该溶液 100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
、Fe3+、Al3+和K+。取该溶液 100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
A、至少存在5种离子 B、Cl-一定存在,且c(Cl-)≥0.4 mol·L-1
C、SO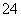 、NH
、NH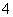 一定存在,Cl-可能不存在 D、CO
一定存在,Cl-可能不存在 D、CO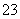 、Al3+一定不存在,K+可能存在
、Al3+一定不存在,K+可能存在
【知识点】离子推断 计算A3 A4 B1 C5 D5
【答案解析】B解析:由于加入过量NaOH溶液,加热,得到0.02mol气体,说明一定有NH4+,且物质的量为0.02mol,同时产生红褐色沉淀,说明一定有Fe3+,1.6g固体为氧化铁,物质的量为0.01mol,则有0.02molFe3+,根据共存知一定没有CO32-;4.66g不溶于盐酸的沉淀为硫酸钡,则溶液中一定有SO42-,物质的量为0.02mol; 根据电荷守恒,一定有Cl-,至少 0.02mol×3+0.02-0.02mol×2
=0.04mol,物质的量浓度至少 0.4mol/L,因此A、C错误;B正确;Al3+无法判断是否存在,D错误。
【思路点拨】根据现象判断可能存在的离子,再根据电荷守恒分析判断存在的其他离子。


科目:高中化学 来源: 题型:
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回到烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入________,目的是
________________________________________________________________________。
(2)反应中加入过量的乙醇,目的是
________________________________________________________________________
________________________________________________________________________。
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加醋酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是__________________
________________________________________________________________________。
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。

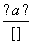
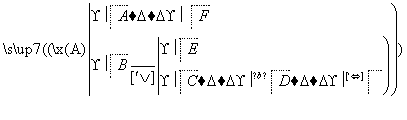
试剂a是____________,试剂b是________;分离方法①是________,分离方法②是________,分离方法③是________________。
(5)在得到的A中加入无水碳酸钠粉末,振荡,目的是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入到FeC12溶液中 ②过量NaOH溶液和明矾溶液馄合 ③少量Ca (OH)2投入过量NaHCO3溶液中 ④向NaAlO2溶液中通入过量CO2 ⑤向饱和Na2CO3溶液中通入过量CO2
A.①②③④⑤ B.只有①④ C.只有②③ D.只有③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
已知硫酸亚铁溶液中加入过氧化钠时发生反应:
4Fe2++4Na2O2+6H2O= 4Fe(OH)3↓+O2↑+8Na+ 则下列说法正确的是( )
A、该反应中 Fe2+是还原剂,O2 是还原产物
B、4molNa2O2 在反应中共得到 8NA 的电子
C、Fe(OH)3 既是氧化产物又是还原产物,每生成 4mol Fe(OH)3 反应过程中共转移电子 6mol
D、反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
.有一种白色粉末由等质量的两种物质混合而成,分别取适量该白色粉末置于三支试管中进行实验。(1)逐滴加入6mol·L-1盐酸,同时不断振荡试管,有气泡产生,反应结束后得到无色透明溶液(2)加热试管中的白色粉末,试管口有水滴凝结(3)逐滴加入6mol·L-1硫酸,同时不断振荡试管,有气泡产生,反应结束后试管中还有白色不溶物。下列混合物中符合以上实验现象的是( )
A.NaHCO3、AgNO3 B.BaCl2、MgCO3 C.NH4HCO3、MgCl2 D.CaCl2·6H2O、Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
(一)(6分)中学常见单质A、B和甲、乙、丙三种化合物有如图所示的转换关系(部分产物未列出)。单质A常作为食品包装材料,甲是两性氧化物。
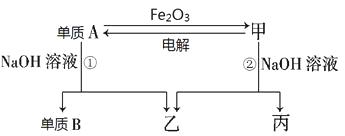
根据图示转化关系回答:
(1)写出下列物质的化学式:单质A_______________,乙_______________。
(2)写出单质A与Fe2O3反应的化学方程式: ,
利用该反应的原理,可用于______________________________。
(3)用单质A做成的容器可以储存和运输浓硫酸的原因是_________________。
(4)写出反应①的离子方程式:_________________________________。
(二)(4分)(5)工业上冶炼下列物质通常不采用电解法的是 。
a.Na b.Mg c.Fe d.Ag
(6)、用铝粉和Fe2O3做铝热反应实验,需要的试剂还有( )
a.KCl b. KClO 3 c. MnO2 d. Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
冶炼金属一般有下列四种方法: ① 焦炭法;② 水煤气(或H2、CO)法;③ 活泼金属置换法;④ 电解法。这四种方法在工业上均有应用。古代有: (Ⅰ) 火烧孔雀石炼铜;(Ⅱ) 湿法炼铜。现代有: (Ⅲ) 铝热法炼铬;(Ⅳ) 从光卤石中炼镁。对它们的冶炼方法的分析中不正确的是(B)
A. (Ⅰ), ①
B. (Ⅱ),②
C. (Ⅲ),③
D. (Ⅳ),④
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气.其中生成NO的能量变化示意图如图1:
①该反应的热化学方程式为
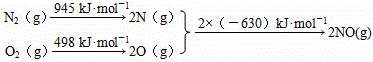 N2(g)+O2(g)=2NO(g)△H=+184kJ•mol﹣1 .
N2(g)+O2(g)=2NO(g)△H=+184kJ•mol﹣1 .
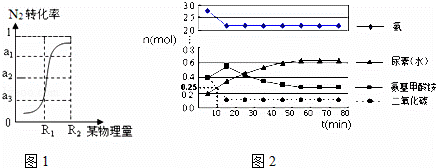
②根据图1所示,只改变条件R,当N2的转化率从a3到a1时,平衡常数K AC .
A.可能增大 B.一定不变 C.可能不变 D.可能减小 E.增大、减小、不变均有可能
(2)尿素(又称碳酰胺)是含氮量最高的氮肥,工业上利用CO2和NH3在一定条件下合成尿素的反应分为:
第一步:2NH3(g)+CO2(g)⇌H2NCOONH4(氨基甲酸铵) (l)
第二步:H2NCOONH4(l)⇌H2O(g)+H2NCONH2(l)
某实验小组模拟工业上合成尿素的条件,在一体积为500L的密闭容器中投入4mol氨和1mol二氧化碳,验测得
反应中各组分的物质的量随时间的变化如图2所示:
①合成尿素总反应的快慢由第 二 步反应决定.
②反应进行到10min时测得CO2的物质的量如上图所示,则用CO2表示的第一步反应的速率v(CO2)= 1.5×10﹣4 mol/(L•min).
③由氨基甲酸铵和CO2曲线变化可得出关于浓度变化和平衡状态的两条结论是:a. 氨基甲酸铵浓度先增大,15min后减小 ;b 15min时第一步反应达到平衡状态,55min第二步反应达到平衡状态 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com