
| A. |  表示某吸热反应分别在有、无催化剂的情况况下反应过程中的能量变化 | |
| B. |  表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的物质的量与NaOH溶液体积的关系,则三种离子的物质的量之比比为(Mg2+):(Al3+):n(NH4+)=2:3:2 | |
| C. | 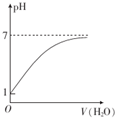 表示常温下0.10 mol•L-1的CH3COOH溶液加水稀释时溶液的pH变化 | |
| D. |  表示向10.00 mL 0.050 mol•L-1盐酸中逐滴加人0.025 mol•L-1的氨水时溶液的pH变化,其中 V1>20.00 |
分析 A.反应物的总能量大于生成物的总能量;催化剂降低反应的活化能;
B.氢氧化钠的体积在0-25mL时,Mg2+、Al3+与NaOH反应生成沉淀;在25-35mL,铵根离子与氢氧化钠反应生成一水合氨;35-40mL时,氢氧化铝与氢氧化钠反应,根据反应物之间的关系计算;
C.醋酸是弱酸,部分电离,醋酸的浓度大于氢离子浓度;
D.氨水与盐酸反应生成氯化铵溶液显酸性,若溶液显中性,则氨水要过量.
解答 解:A.吸热反应,反应物的总能量小于生成物的总能量,而图中反应物的总能量大于生成物的总能量,是放热反应,催化剂降低反应的活化能,故A错误;
B.氢氧化钠的体积在0-25mL时,Mg2+、Al3+与NaOH反应生成沉淀,Al3++3OH-=Al(OH)3↓、Mg2++2OH-=Mg(OH)2↓;在25-35mL,铵根离子与氢氧化钠反应生成一水合氨,NH4++OH-=NH3•H2O;35-40mL时,氢氧化铝与氢氧化钠反应,Al(OH)3+OH-=AlO2-+2H2O,NH4+消耗的NaOH的体积是Al(OH)3消耗的NaOH体积的2倍,则NH4+的浓度是Al3+浓度的2倍,故B错误;
C.醋酸是弱酸,部分电离,醋酸的浓度大于氢离子浓度,所以常温下0.10 mol•L-1的CH3COOH溶液中氢离子浓度小于0.1mol/L,所以pH大于1,故C错误;
D.向10.00 mL 0.050 mol•L-1盐酸中逐滴加人0.025 mol•L-1的氨水时,当氨水与盐酸恰好反应生成氯化铵溶液显酸性,若溶液显中性,则氨水要过量,所以V1>20.00,故D正确.
故选D.
点评 本题考查了化学反应的能量变化图、弱电解质的电离、离子反应及图象的分析计算,题目难度中等,把握弱电解质的电离特点、溶液中发生的反应及与图象的对应关系为解答的关键,侧重分析与推断能力的考查.


科目:高中化学 来源: 题型:解答题
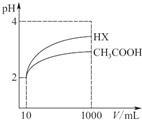 请根据下表,回答下列问题:(数据均在25℃时测定)
请根据下表,回答下列问题:(数据均在25℃时测定)| 化学式 | CH3COOH | H2CO3 | HClO | Cu(OH)2 |
| 相关常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 | Ksp=2×10-20 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
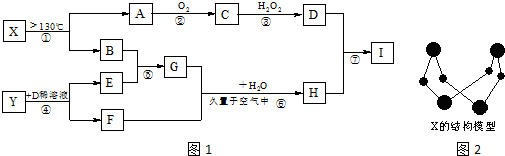
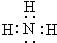 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
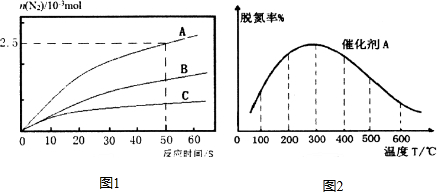 研究发现,NOx是雾霾的主要成分之一,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.
研究发现,NOx是雾霾的主要成分之一,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
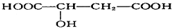 ,苹果酸可能发生的反应是( )
,苹果酸可能发生的反应是( )| A. | ①②③ | B. | ①②③④ | C. | ①②③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
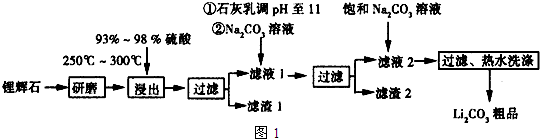
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
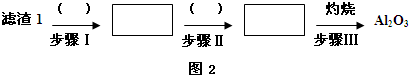
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com