
【题目】光刻胶是制造芯片、集成电路的关键材料,其中KPR胶的一种合成路线如下:
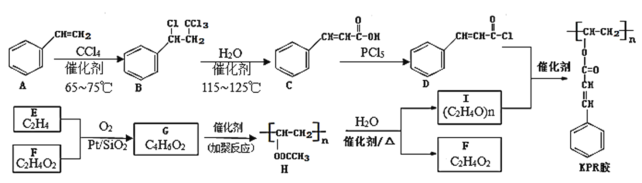
(1)①A→B、C→D的反应类型依次为__________ 、__________。
②C中的官能团名称是__________和__________。
(2)由E为起始原料制备F的一种流程为:
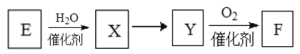
则X转化为Y所需的试剂和条件依次是__________ 、__________。
(3) G的结构简式为_________。
(4)写出反应H+H2O→I+F的化学方程式:_____________(有机物用结构简式表示)。
【答案】加成反应 取代反应 碳碳双键 羧基 催化剂(Cu或Ag) 加热 CH3COOCH=CH2 ![]() +n H2O
+n H2O![]()
![]() + n CH3COOH
+ n CH3COOH
【解析】
![]() 水解为
水解为![]() 和CH3COOH,I是
和CH3COOH,I是![]() 、F是CH3COOH;G发生加聚反应生成
、F是CH3COOH;G发生加聚反应生成![]() ,G是CH3COOCH=CH2;E的分子式是C2H4,E是CH2=CH2;
,G是CH3COOCH=CH2;E的分子式是C2H4,E是CH2=CH2;
(1)①A→B是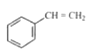 中碳碳双键断,双键两端的碳原子直接与氯原子、-CCl3相连生成
中碳碳双键断,双键两端的碳原子直接与氯原子、-CCl3相连生成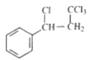 ,属于加成反应;C→D是
,属于加成反应;C→D是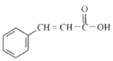 中的-OH被氯原子代替生成
中的-OH被氯原子代替生成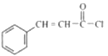 ,反应类型是取代反应;
,反应类型是取代反应;
②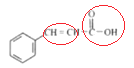 中的官能团名称是碳碳双键和羧基;
中的官能团名称是碳碳双键和羧基;
(2)E是CH2=CH2,乙烯和水反应生成乙醇、乙醇氧化为乙醛、乙醛氧化为乙酸,F是乙酸,乙醇在铜或银作催化剂的条件下加热被氧气氧化为乙醛,则乙醇转化为乙醛所需的试剂和条件依次是催化剂(Cu或Ag)、加热;
(3) G发生加聚反应生成![]() ,逆推可知G的结构简式为CH3COOCH=CH2;
,逆推可知G的结构简式为CH3COOCH=CH2;
(4) ![]() 水解为
水解为![]() 和CH3COOH,反应的化学方程式为
和CH3COOH,反应的化学方程式为![]() +n H2O
+n H2O![]()
![]() + n CH3COOH。
+ n CH3COOH。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】用下列实验装置进行的实验,能达到相应实验目的的是()
A. 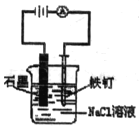 防止铁钉生锈
防止铁钉生锈
B. 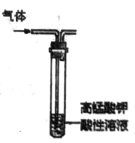 除去乙烷中混有的乙烯
除去乙烷中混有的乙烯
C. 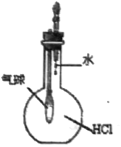 验证HCl气体在水中的溶解性
验证HCl气体在水中的溶解性
D. 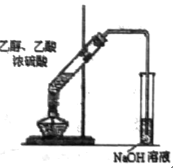 实验室制取乙酸乙酯
实验室制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是_______________________________________。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式。
C6H12O6(葡萄糖)![]() 2________+2C2H5OH
2________+2C2H5OH
(3)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是________________________________。
②试管b中盛放的试剂是饱和_________________溶液。
⑧实验开始时,试管b中的导管不伸入液面下的原因是___________________。
④若分离出试管b中生成的乙酸乙酯,需要用到的仪器是____(填序号)。
a. 漏斗 b. 分液漏斗 c. 长颈漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】仪器保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)和PVDC.其中PE和PVDC是安全的,PVC对人体有潜在危害.工业上用乙烯和氯气为主要原料来合成上述三种物质。
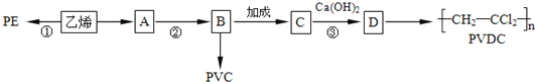
完成下列填空:
(1)A的名称__;反应①的类型__;
(2)反应②的反应条件__;D的同分异构体的结构简式__;
(3)反应③的化学方程式_______;
(4)反应②中有多种副反应,得到的有机副产品除了CH3CHO和![]() 外,还可能有_______。
外,还可能有_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 X、Y、Z、W 原子序数依次增大,X 是地壳中含量最多的元素,Y 原子的最外层只有一个电子,Z 位于元素周期表ⅢA族,W 与X属于同一主族。下列说法正确的是
A. 原子半径:r(W) > r(Z) > r(Y)
B. 由X、Y 组成的化合物中均不含共价键
C. Y 的最高价氧化物的水化物的碱性比Z的弱
D. X 的简单气态氢化物的热稳定性比W的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极完成下列电解实验。
实验一 | 实验二 | |
装置 |
|
|
现象 | a 、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近均有气泡产生;铜珠n的右侧有气泡产生。 |
下列对实验现象的解释或推测不合理的是( )
A. 根据实验一的原理,实验二中铜珠m左侧变厚
B. a、d处:2H2O+2e-=H2↑+2OH-
C. b处:2Cl--2e-=Cl2↑;Cl2 + H2O =HCl + HClO
D. c处发生了反应:Fe-2e-=Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:X2(g)+3Y2(g)2Z(g),其中 X2、Y2、Z 的起始浓度分别为0.1 mol·L-1、0.4 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
A.c(Z)=0.4 mol·L-1B.c(Y2)=0 mol·L-1
C.c(X2)=0.2 mol·L-1D.c(X2)=0.05 mol·L-1 且 c(Z)=0.3 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高碘酸钾(KIO4)溶于热水,微溶于冷水和氢氧化钾溶液,可用作有机物的氧化剂。制备高碘酸钾的装置图如下(夹持和加热装置省略)。回答下列问题:

(1)装置I中仪器甲的名称是___________。
(2)装置I中浓盐酸与KMnO4混合后发生反应的离子方程式是___________。
(3)装置Ⅱ中的试剂X是___________。
(4)装置Ⅲ中搅拌的目的是___________。
(5)上述炭置按气流由左至右各接口顺序为___________(用字母表示)。
(6)装置连接好后,将装置Ⅲ水浴加热,通入氯气一段时间,冷却析岀高碘酸钾晶体,经过滤,洗涤,干燥等步骤得到产品。
①写出装置Ⅲ中发生反应的化学方程式:___________。
②洗涤时,与选用热水相比,选用冷水洗涤晶体的优点是___________。
③上述制备的产品中含少量的KIO3,其他杂质忽略,现称取ag该产品配制成溶液,然后加入稍过量的用醋酸酸化的KI溶液,充分反应后,加入几滴淀粉溶液,然后用1.0mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液的平均体积为bL。
已知:KIO3+5KI+6CH3COOH===3I2+6CH3COOK+3H2O
KIO4+7KI+8CH3 COOH===4I2+8CH3COOK+4H2O
I2+2Na2S2O3===2NaI+N2S4O6
则该产品中KIO4的百分含量是___________(Mr(KIO3)=214,Mr(KIO4)=230,列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
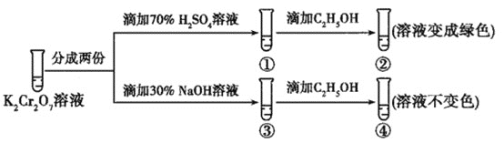
结合实验,下列说法不正确的是( )
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr2O72-被C2H5OH还原
C.对比②和④可知K2Cr2O7酸性溶液氧化性强
D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com